遗传谱系学视域下的孔子后裔问题再认识
2026年5月11日古基因组揭示东亚 16 万年人群动态演化与生物适应机制
何广林、孙云涛、段书涵、罗林涛、孙秋霞、李博文、云立兵、刘超、王梦格
摘要
古DNA研究的进步彻底改变了人类对自身演化、人群混合驱动适应以及性状遗传基础的认知。然而,旧石器时代与新石器时代东亚人群的演化脉络仍较为零散。本文综述梳理了16万年间的人群互动历史,重点阐释三次古老人群基因渗入事件与大规模人群混合现象。文章探讨古老谱系与农业革新如何塑造东亚人群格局,同时与生计方式变迁相关的迁徙和人群混合事件,推动了人类基因组与表型多样性的形成。古基因组中的适应性遗传特征,进一步阐明了人类高海拔适应、肤色色素沉着及体质形态特征的遗传底层机制,为人类演化生物学提供了全新研究视角。
引言
近二十年来,得益于DNA捕获技术、测序技术、标准化实验流程与生物信息学分析方法的革新,古DNA研究取得长足发展[1, 2]。依托古基因组以及语言族群多样的现代人群大规模基因组数据,学界对解剖学现代人类及其近亲(尼安德特人、丹尼索瓦人)的演化路径有了更为深刻的认知[3]。这些研究成果为解析人类起源与演化进程、复杂人群混合与遗传交流、不同时空古人群的生物适应性,以及现代不同地域人群健康与疾病特征的遗传基础等关键科学问题,提供了宝贵研究视角[4]。尽管成果丰硕,现有研究多聚焦人类演化关键节点,例如走出非洲、早期定居模式,以及欧亚大陆西部、西伯利亚、大洋洲和美洲的后续迁徙与人群混合事件[1]。但研究长期过度偏向欧洲人群,导致人类演化整体认知存在显著偏差[5]。
针对东亚与北亚(西伯利亚及周边)旧石器时代晚期人群的基因组研究,极大推进了学界对现代人类谱系早期分化、走出非洲后对现代人群遗传多样性及古老基因渗入贡献的理解[1]。2010年尼安德特人与丹尼索瓦人基因组的成功测序,为解析这两类古老古人类与现代非洲以外人群的遗传亲缘关系提供了关键依据[6,7,8]。与单亲遗传物质不同,常染色体基因组数据可清晰佐证遗传关联,印证其与现代人类拥有共同祖先谱系[9, 10]。基于共有遗传变异的谱系重建显示,古老古人类与现代人类约在55万年前发生谱系分化,尼安德特人与丹尼索瓦人则约在40万年前相互分化[11,12,13]。单倍型多样性特征进一步揭示了古老基因渗入的复杂性:尼安德特人渗入片段在全球不同地域人群中多样性低、含量与长度相对均一,提示仅发生一次大规模基因渗入事件;而丹尼索瓦人相关单倍型多样性极高,在澳洲原住民、美拉尼西亚人、菲律宾尼格利陀人及其他亚洲、美洲人群中,匹配率、基因含量与片段长度均存在明显差异[6,7,8],说明丹尼索瓦人基因渗入历史更为复杂多元[3]。统计估算显示,非洲以外人群平均携带约2.5±0.6%的尼安德特人祖先成分,美拉尼西亚人与菲律宾尼格利陀人丹尼索瓦人祖先占比约5%[14]。古DNA研究进一步证实,适应性基因渗入在人类演化中扮演关键角色,通过引入有利遗传变异,助力人类快速适应全新环境[15]。这些基因组研究成果持续深化了人类演化史认知,以及现代人群与古老人群间的遗传互作机制。
全新世以来,多数古DNA研究聚焦欧亚大陆、大洋洲与美洲的跨大陆人群迁徙,这类迁徙与农业扩张、语言扩散密切相关[16]。古DNA数据重塑了学界对欧洲人群遗传多样性的认知,证实现代欧洲人的基因库主要由三大祖先成分构成:近东农耕人群、颜那亚相关游牧人群及本地狩猎采集人群[17]。此外,西伯利亚古DNA证实了复杂的人群互动过程,以及古北欧欧亚人、古东北亚人、古古西伯利亚人、新西伯利亚人与古北西伯利亚人等不同遗传祖先成分的更替[18]。人类遗骸DNA的获取与测序,也推动了美洲早期人类定居、南北美洲原住民谱系分化、北美南北印第安人群分离、旧石器时代人群向大洋洲迁徙,以及新石器时代南岛语人群向瓦努阿图扩张等议题的研究[4, 19]。
东亚(含中国、蒙古、日本及周边区域)留存大量历史遗迹与考古人类遗骸,人类遗传数据成为解析人类起源关键问题、破解人群健康相关谜团的核心资源[20,21,22,23,24]。依托生物样本库队列的遗传数据,已成为国家重要战略资源,也是解析人类遗传历史、阐释疾病与健康遗传演化决定因素的核心工具[25]。但目前结合东亚古、现代人群基因组数据,追溯人类起源演化脉络与适应性遗传变异的研究仍相对匮乏。统计分析显示,东亚大规模古DNA样本储备严重不足,艾伦古DNA资源库中时空差异化古DNA样本不足1000例(图1A-C)[26]。因此,系统梳理中国古人群完整演化历史与生物适应进程具有重要研究价值。
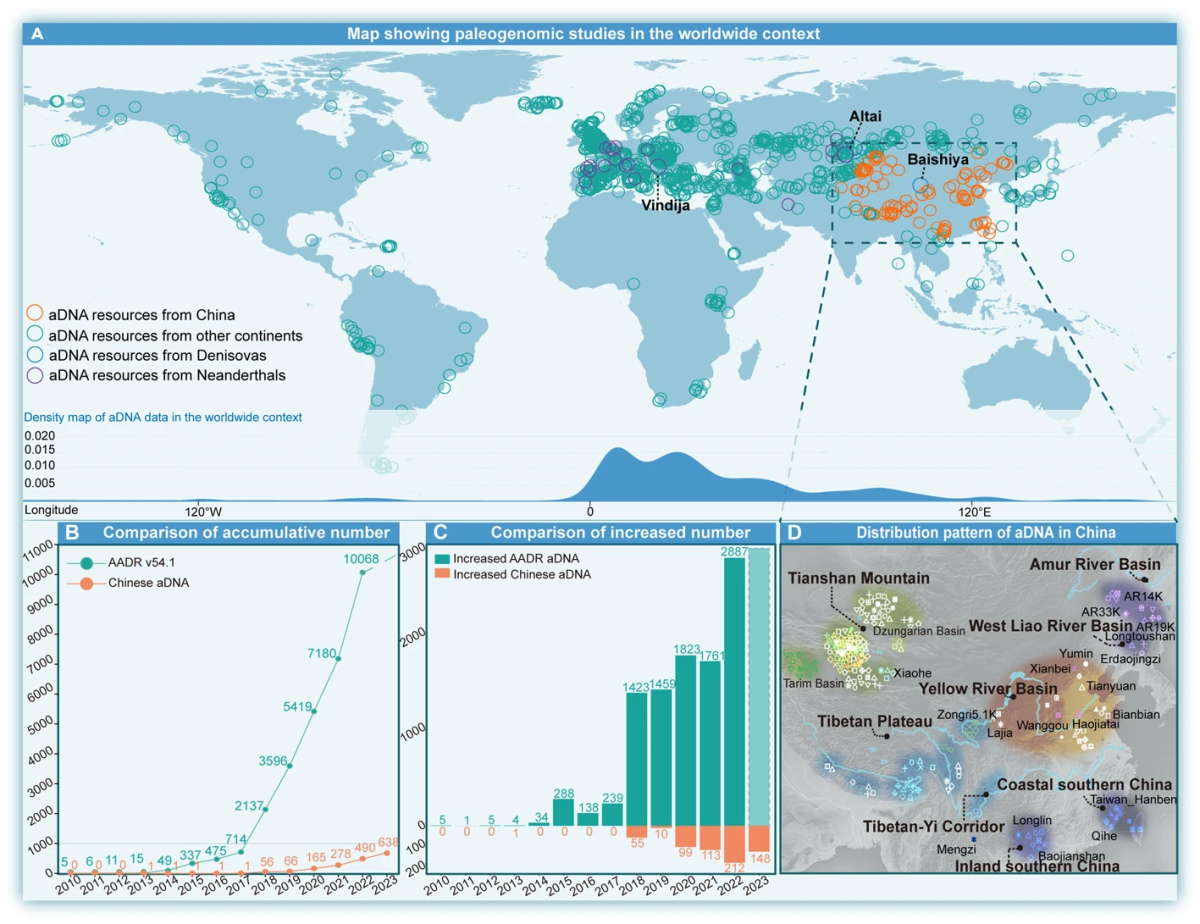
本文系统梳理不同生态区古DNA研究最新进展,涵盖低海拔农业起源核心区(黄河流域、长江流域、西辽河流域),以及极端环境高海拔区域(青藏高原及藏彝走廊);同时纳入横跨西伯利亚、欧亚西部与中国北方的跨界区域(天山山脉、蒙古高原、黑龙江流域)相关研究(图1D)。文章从更新世至全新世,多角度阐释东亚古人群历史演化与生物适应规律,并围绕七大核心主题展开综述:(Ⅰ)尼安德特人与丹尼索瓦人的古老基因渗入:解析古老谱系对东亚人群基因库的贡献,重点梳理两类古老人群的基因渗入事件。(Ⅱ)东亚早期人类定居与亚洲基础祖先谱系:梳理更新世东亚核心古人群谱系,阐释东亚早期人类定居历程。(Ⅲ)粟作与稻作农耕人群的南北分化及人群动态:探讨旧石器时代古东亚南、北人群遗传分化,以及新石器时代黄河粟作人群与长江稻作人群扩张引发的人群混合格局。(Ⅳ)高原古人群遗传结构:解析青藏高原古人群遗传组成,以及中国西南混合农耕古人群的遗传亲缘关系。(Ⅴ)跨欧亚区域古农耕与古游牧人群的遗传交流:探讨中国西北古人群遗传连续性,以及中国东北生计方式变迁对应的人群结构更替。(Ⅵ)古DNA揭示的生物适应及其对人类健康与疾病的影响:总结人类健康与疾病的演化遗传决定因素,重点分析古人群不同时空下等位基因演变规律。(Ⅶ)古DNA技术革新与复杂社会组织重建:展望古DNA未来技术发展方向,及其在重建古人类社会组织中的应用前景。
16万年古老谱系及其对古今现代人类的遗传影响
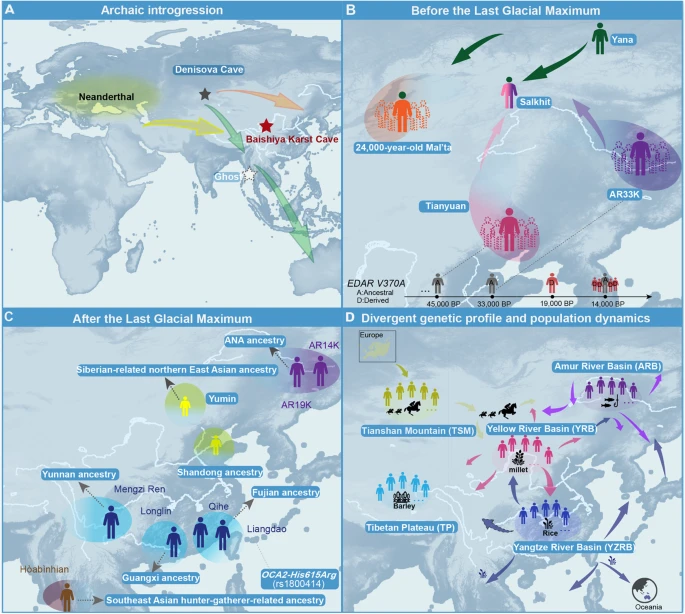
尼安德特人与丹尼索瓦人因与现代人类演化关系密切、且曾与人类祖先存在族群互动,一直是学界研究热点[13]。但受限于骨骼形态与遗传数据匮乏,学界难以厘清其通过基因渗入在东亚人群中留下的遗传印记。已有研究通过古蛋白分析,在甘肃白石崖溶洞鉴定出丹尼索瓦人下颌骨化石,证实中更新世时期古老古人类已栖息于青藏高原东北部,远早于现代人群抵达,并已成功适应高海拔低氧环境[27]。从白石崖溶洞沉积物中提取的线粒体DNA,佐证距今10万至6万年间丹尼索瓦人已在此栖息[28]。距今14.6万年哈尔滨头骨化石的线粒体基因组与古蛋白质组研究表明,中更新世晚期黑龙江流域已存在丹尼索瓦人谱系[29, 30]。针对古老基因渗入的深入研究,证实了古老古人类与现代人类间的遗传交流,人类通过获取有利遗传变异提升了新环境下的生存能力[31]。具体而言,遗传研究已重构出现代中国人群(尤其藏族)经历的三次古老基因渗入浪潮[32]:一次尼安德特人基因流发生在非洲以外人群谱系分化之前;同时识别出两次独立的丹尼索瓦人混合事件,一次与大洋洲人群共享,另一次为东亚人群特有[15, 32]。值得注意的是,东亚人群与古老古人类的特有接触,促使适应性基因片段渗入现代人类,例如藏族人群中源自丹尼索瓦人的EPAS1基因变异[33]。通过单倍型共享分析鉴定出的5个SNP核心丹尼索瓦人单倍型,在现代藏族人群中广泛分布,支撑了藏族对极端高原环境的快速适应[33]。古基因组研究还发现,古老基因渗入可影响人体药物及内源物质代谢,为基于易感基因开发精准靶向治疗药物提供了理论基础[25]。
目前针对古老古人类的研究,已证实适应性基因渗入在中国古今人群中留下了深远遗传印记。但现有研究仅初步勾勒早期人类遗传历史框架,仍存在诸多研究空白亟待填补。随着DNA提取与测序技术迭代,亟需从金牛山、许家窑、许昌、澎湖、郧县等具有丹尼索瓦人形态特征的旧石器古人类遗存中获取高质量基因组数据[34]。这类数据能够完善东亚更新世人类演化全景图谱,厘清这些遗传独立或存在关联的古老人群与现代东亚人群的遗传亲缘及混合历程。想要全面评估丹尼索瓦人、尼安德特人及其他超古老祖先成分的混合比例,还需更多古老人类高深度基因组数据,才能深入解析古老祖先对现代人类的遗传塑造作用。
中国东北与华南地区更新世深层古老谱系
学界对更新世人类遗传结构与人群分化格局的认知仍十分有限。人群更替与迁徙是欧洲旧石器时代历史的核心特征[35]。但受限于古人类化石遗传样本稀缺,同一时期东亚人群演化史,尤其是末次盛冰期前后的人群变迁脉络,仍零散且模糊[1, 36]。依托末次盛冰期前古人类高质量基因组数据,学界对北京周口店距今4万年的田园洞个体、黑龙江流域距今3.36万年AR33K女性样本开展了遗传解析(图2)。基于等位基因共享的人群混合与谱系演化模型,为解析中国北方解剖学与行为学现代人类史前定居格局奠定了基础。遗传模型显示,这类古人群是东亚北方人群的基础祖先谱系,且其基因组中丹尼索瓦人基因渗入比例显著高于现代及其他古人群[37]。尽管旧石器时代AR33K人群与田园洞人群遗传相似度较高,但AR33K并未像田园洞人群那样与西欧亚古人群(如比利时GoyrtQ116-1个体)、现代美洲原住民(如亚马逊苏鲁伊人)存在遗传亲缘关联[38, 39]。与贝加尔湖附近白拉亚河距今2.4万年MA-1人群遗传近缘的田园洞/AR33K相关祖先谱系,曾广泛分布于东亚北部与西伯利亚,在末次盛冰期前已形成复杂人群结构[40,41]。
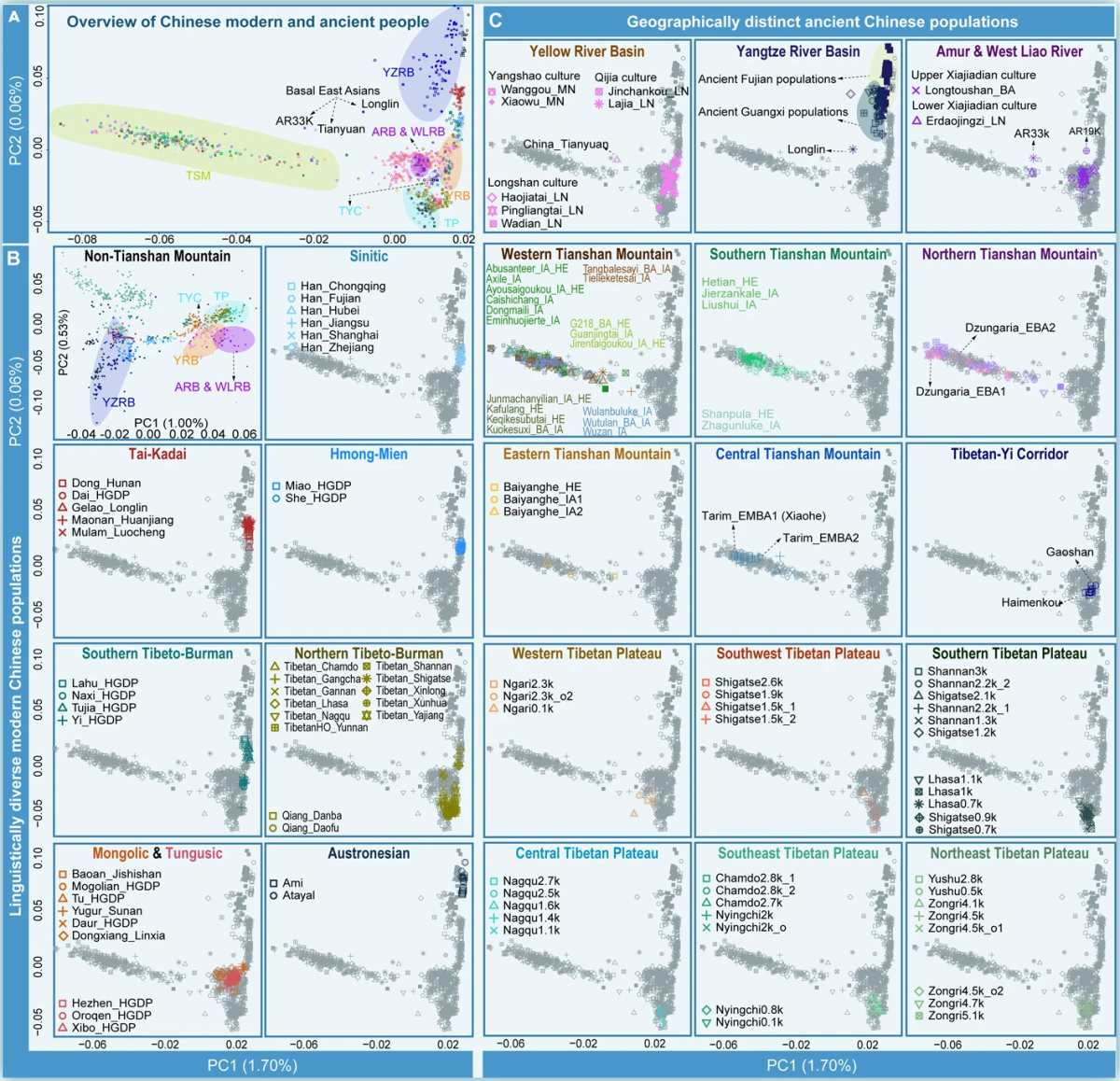
在西伯利亚与东亚交汇地带,末次盛冰期前后发生了大规模人群遗传更替。已有研究识别出末次盛冰期末期栖息于黑龙江流域的AR19K人群,是目前已知最早的古东北亚人群,其遗传结构独特,与田园洞/AR33K相关祖先谱系完全分化[41]。东亚其他区域(尤其农业起源核心区)末次盛冰期前人群遗传数据仍十分匮乏。近年陆续报道了东亚南部三份晚旧石器时代古基因组:距今1.4万年的云南蒙自人(马鹿洞)、距今11747–11356年的奇和3号个体、距今10686–10439年的广西隆林人(捞冒草洞)[42, 43]。双层起源假说认为,华南与东南亚古狩猎采集人群,由和平文化相关亚洲深层古老祖先与华南新石器农耕人群共同塑造[44]。基因组分析表明,蒙自人代表一支独立于和平文化谱系的东亚南部早期分化古老谱系,且在晚更新世对首批美洲人群基因库存在遗传贡献[43]。广西隆林人头骨兼具古老古人类与早期现代人类形态特征;古DNA分析显示,其遗传归属落入现代东亚人群多样性范畴,与亚洲各分化古老谱系均为远缘关联[42]。奇和3号个体与福建新石器人群(奇和2号、亮岛1号、亮岛2号)遗传亲缘关系密切,人群演化模式不同于携带广西隆林、云南蒙自及越南和平文化祖先成分的其他旧石器人群[42]。目前遗传与考古证据不足,难以获取兼具时空分辨率的旧石器人类直接基因组数据。因此,亟需开展系统综合研究,厘清末次盛冰期前及旧石器时代早期人群演化历史,阐释其扩散与谱系更替规律。
基于农民相关古基因组推断的南北遗传分化与种群动态
新石器时代转型以狩猎采集、游牧和渔猎生计方式向农业转变为标志,伴随着复杂的种群迁徙、混合事件、语言分化以及复杂社会结构的形成。中国作为最早的农业驯化中心之一,见证了黄河流域(YRB)粟作农业的兴起,包括粟(Setaria italica)和黍(Panicum miliaceum)的种植[45],以及长江流域(YZRB)以栽培稻(Oryza sativa ssp. japonica)为代表的稻作农业发展[46]。这些农业实践的扩张与中国北方原始汉藏语系的扩张和分化,以及中国南方超语系的扩散密切相关[47, 48]。语言学、考古学和遗传学证据为汉藏语系人群及其祖先的遗传起源和祖源构成提供了线索[49, 50]。Zhang等人刻画了不同语系群体间的系统发育关系,将汉语族和藏缅语族人群与新石器时代仰韶文化、龙山文化的扩张以及马家窑/齐家文化的西传联系起来[49]。同样,Sagart等人重建了汉藏语系的系统发育拓扑结构,并通过分化时间估算证实,汉藏语系与中国北方晚磁山文化和早仰韶文化的粟作农民直接相关,可追溯至距今约7200年(BP)[51]。
粟作农民的基因组历史
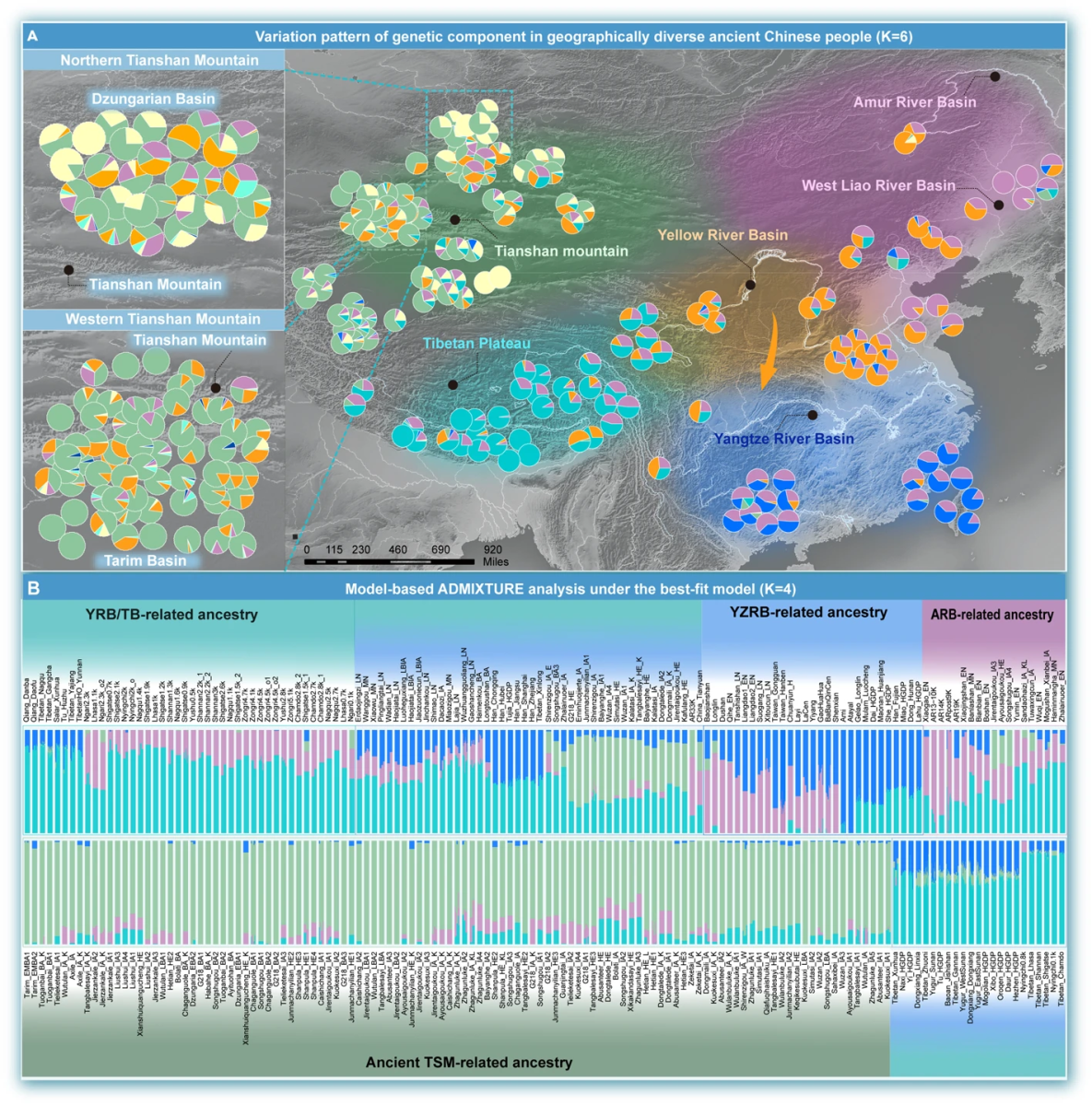
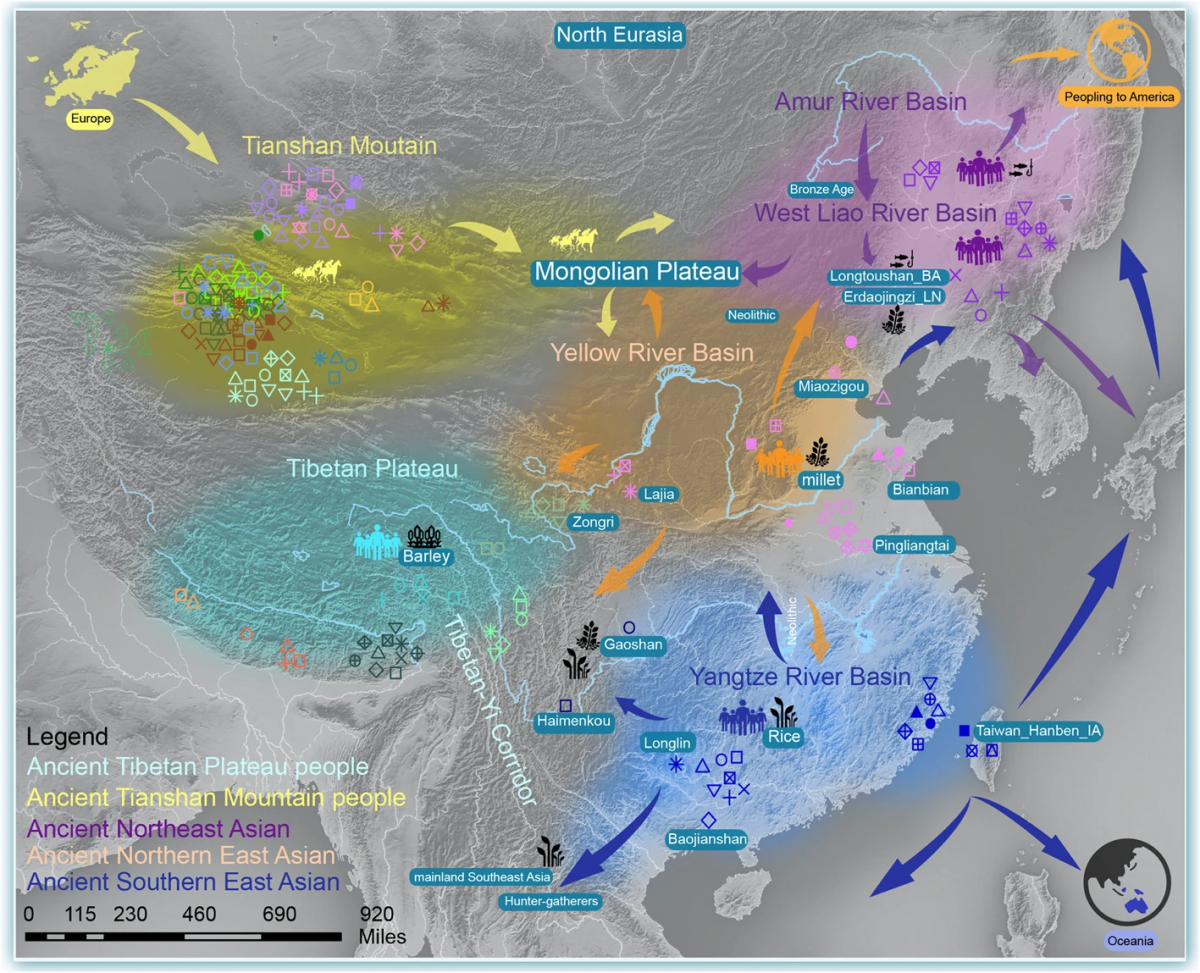
来自安纳托利亚、黎凡特和伊朗扎格罗斯山脉的古代近东人群的长距离时空迁徙表明,遗传分化的早期农民首先相互混合,随后向近东以外地区扩散,对东非、欧亚草原、欧洲和南亚的遗传构成产生了重大影响[52]。来自黄河流域上游(甘肃、青海、陕西)、中游(河南)和下游(山东)地区的古基因组反映了类似的种群转变,并受到周边人群的遗传影响[50, 53,54,55,56,57,58]。Yang等人报道了来自山东的古DNA,包括来自扁扁洞、小高、博山和小金山的早期新石器时代古代东北亚(ANEA)个体,揭示了与西伯利亚狩猎采集人群亲缘关系密切的沿海古代东北亚谱系[54]。Du及其合作者分析了山东从中新石器时代到历史时期的古基因组,揭示了复杂的区域种群动态[55, 58]。这些发现强调了新石器时代粟作农民对大汶口人群的遗传贡献、大汶口与龙山人群之间的人群扩散,以及历史时期人群间复杂的混合模式[55, 58]。同样,Li等人研究了仰韶村遗址的古基因组数据,并将其与中原地区时空多样的基因组整合分析[56, 57]。种群混合模型表明,尽管存在复杂的区域文化和人口互动,但仰韶人群与其中原后裔之间保持着长期的遗传稳定性[56, 57]。黄河流域上游距今约3000年的新石器时代五庄果墚相关祖源贡献了藏族基因库的约84%,以及现代汉族人群的59%-84%,这些汉族人群也与地理上邻近的裕民人群有着密切的遗传联系(图 2)[50]。Ning等人分析了来自黄河流域和西辽河流域(WLRB)的最早一批粟作农民相关基因组数据集(图 3),并指出这些人群的遗传分层与生计方式转变相关[53]。该研究强调,中新石器时代仰韶文化、王湾和小五人群与晚新石器时代龙山人群之间的粟作相关遗传遗产呈平行增长趋势,同时晚新石器时代齐家文化相关祖源(金禅口和喇家)在现代藏缅语族人群中存在,这表明汉藏语系人群共同起源于黄河流域[53]。Wang等人进一步证实了汉藏语系人群共同起源于中国北方[50]。随后,对古代黄河流域相关基因组和现代基因组的联合分析揭示了不同地理区域黄河流域人群的遗传稳定性和连续性[59, 60]。从古基因组推断的种群历史进一步阐明了中国境内遗传更替与生计方式转变之间的关联。Ning等人证明,黄河流域北部粟作农民的人群扩散显著影响了西辽河流域早期夏家店人群的遗传构成,而后期的游牧人群祖源则对后续世代产生了贡献[53]。粟作农民的扩张被认为向西传播到了青藏高原(TP)和河西走廊(HXC),向北传播到了欧亚草原和西辽河流域,向东传播到了日本和朝鲜半岛,向南传播到了长江流域和藏彝走廊(TYC)[47, 50, 54, 61]。未来对黄河流域本地旧石器时代狩猎采集人群的研究将为农业起源以及狩猎采集社会向粟作农业社会的转变提供宝贵线索(图 4)。
稻作农民的遗传遗产及其对东南亚人群的影响
来自仙人洞和跨湖桥遗址的考古研究表明,中国南方存在两种不同的长江流域稻作传统,一种主要分布在沿海地区,另一种主要分布在内陆地区。从福建和广西个体中提取的古DNA遗传证据证实了这一区别[42, 54]。中国东南部东亚祖源的遗传特征也已得到阐明。Yang等人最近对位于长江中游北缘的八里岗遗址从中新石器时代到晚青铜时代的58个个体进行了基因组测序。这些发现表明,八里岗人群在不同时期经历了多波次的混合,交替呈现向南和向北的基因流动[62]。Xiong等人在长江中下游关键区域识别出了来自福泉山、马桥和大溪人群的关键古基因组,表明长江流域新石器时代人群与原南岛语系人群之间存在直接遗传联系[47]。Yang等人分析了长江流域南部地区的19个古代沿海基因组,报告称这些个体主要携带东亚相关祖源[54]。值得注意的是,距今8400-7500年的奇和洞和亮岛早期新石器时代人群的颅骨形态最初被认为与狩猎采集人群密切相关[63],但古DNA证据后来推翻了这一假设[54]。Wang等人对来自中国南方(广西和福建)的31个古基因组进行了测序,揭示了广西新石器时代人群与福建、云南和越南早期新石器时代遗址人群之间存在显著遗传差异[42]。距今9000-6000年的中新石器时代狩猎采集者呈现出三种不同的祖源来源,包括广西(独山和宝剑山)以及福建和越南邻近地区人群的贡献[42]。通过基因组分析证实,距今1500-500年的广西历史人群高花花和八板琴岑与现代壮侗语族和苗瑶语族人群具有很强的遗传亲缘性[42]。此外,Wang等人报告称,距今3300-1200年的台湾古代人群(卑南和公馆)约75%的祖源来自长江流域稻作相关农民。这些原南岛语系相关古代人群,如铁器时代卑南人群,与中国南方现代壮侗语族人群共享大量遗传等位基因(图 2B和 2)[50]。
黄河流域和长江流域之间的双向基因流动促进了稻粟混作农业系统沿沿海、中部和内陆走廊的传播[47, 62]。Ning等人指出,河南的龙山文化及后来的洛河骨巷人群比地理上邻近的仰韶人群携带更多与中国南方东亚人相关的等位基因[53](图 3)。Wang等人随后报道的中国南方沿海古DNA数据[42]揭示了距今6400-1500年间北方祖源相关的迁徙,这一模式在福建新石器时代昙石山和溪头村人群中也得到了验证[54]。最近对云贵高原大松山遗址公元990-1649年古基因组的大规模分析显示,该地区存在大量黄河流域相关祖源[64, 65]。显然,类似的双向遗传混合模式也存在于八里岗人群和长江中下游其他古代群体中[47, 62]。这些发现表明,来自中原的汉族祖先人群扩散对中国南方的基因库产生了重大影响[65]。此外,三角验证证据支持生计方式与人类迁徙之间的联系,表明农业和语言从黄河流域的原汉藏语系人群传播到了西辽河流域的粟作农业中心[53, 66],以及中原和草原群体[67]。通过全基因组古DNA数据进行的综合遗传分析可以揭示过去的种群动态,特别是与农民扩张相关的语言和农业在中国境内外的共同扩散[4, 50]。此外,Wang等人提出了一个值得注意的混合场景,涉及距今约9000-6000年、农业出现之前携带长江流域相关祖源的古代个体[42]。这种混合与中国南方本地祖源以及东南亚和平文化(Hòabìnhian)狩猎采集者的深层亚洲祖源相关(图 4)。
遗传证据表明,史前东南亚人群的形成涉及来自中国南方的五次不同的向南迁徙[44, 68]。这些迁徙促进了南岛语系和壮侗语系在沿海地区的扩散,以及苗瑶语系、南亚语系和藏缅语系在内陆地区的传播。此外,Yang等人发现中国南方长江流域稻作农民与大洋洲拉皮塔文化之间存在遗传联系,表明原南岛语系祖先起源于中国南方,并随着稻作农业的扩张而扩散[54]。Wang等人报告称,携带长江流域稻作农民相关祖源的个体的移动与南岛语系、苗瑶语系和壮侗语系群体的扩散同时发生[50]。总的来说,这些发现凸显了古代农民群体之间基因流动的普遍性,强调了中国西南地区、东南亚大陆、中国南方沿海地区、西伯利亚、日本、越南和大洋洲之间的遗传联系(图 4)[42, 50, 54]。末次冰盛期(LGM)之后,气候向温暖环境转变,推动了中国古代人群频繁的种群动态变化。这包括一系列人群与文化的共同扩散,以及南北迁徙和中国境外的互动。然而,目前的采样仅限于少数中国古代个体,特别是来自温暖湿润环境的长江流域中上游稻作农民。这种采样偏差可能无法完全捕捉这些人群的遗传多样性和人口历史。
新石器时代以来中国北方与欧亚草原东部交汇地带的动态种群历史
欧亚草原西部与蒙古高原(MP)东部狩猎采集人群之间的旧石器时代分离,以及青铜时代大规模的西向迁徙,是欧亚草原历史的核心主题[69]。这些迁徙包括颜那亚(Yamnaya)、阿凡纳谢沃(Afanasievo)、切木尔切克(Chemurchek)和辛塔什塔(Sintashta)文化人群的移动,以及程度较轻的巴克特里亚-马尔吉亚纳考古综合体(BMAC)相关大麦农民的迁徙。青铜时代之后的迁徙,如匈奴、鲜卑、柔然、突厥和蒙古等游牧政权的迁徙,进一步塑造了欧亚草原的人口格局。除了这些大规模迁徙外,俄罗斯远东地区、黑龙江流域西部的魔鬼洞和博伊斯曼新石器时代人群以及现代通古斯语族人群中观察到的长期遗传稳定性也值得注意。西伯利亚狩猎采集者或游牧者与黄河流域粟作农民之间的广泛互动也显著影响了这些农牧交错带内古代和现代人群的遗传多样性和种群结构。本综述总结了西伯利亚、中亚和中国北方交汇地带的种群历史和人口模式,这些地区共享的古代遗传和文化元素,包括小麦、大麦、粟、开菲尔奶酪、青铜技术、牛和羊/山羊,反映了广泛的跨欧亚文化和种群交流[2, 70]。这些元素也暗示了共同的阿尔泰语系或跨欧亚语系,包括突厥语族、蒙古语族和通古斯语族。在本研究中,这些交汇地带统称为”跨欧亚地区”,包括中国北方及邻近地区的天山山脉、蒙古高原、黑龙江流域和西辽河流域。这些地区位于关键的生态交错带,是定居粟作农业者和游牧畜牧者交汇的地方(图 1D)。这些地区是多个古代文明的摇篮,促进了不同复杂社会之间物质文化、农业技术和生计方式的交流[71]。
古代天山山脉人群的复杂混合
阿尔泰山脉是早期跨欧亚种群迁徙和文化交流的主要屏障。同样,位于中国新疆中西部的天山山脉将阿尔泰山脉南部分为北疆和南疆,分别涵盖准噶尔盆地和塔里木盆地。古代天山山脉地区拥有来自原始印欧语系人群的深层遗传谱系,特别是塔里木盆地的吐火罗语族人群,以及在自然木乃伊化的人类遗骸中观察到的复杂的东西方体质特征[72]。新疆维吾尔自治区作为中国西北历史上至关重要的地理走廊,自汉代(距今约2200-1800年)以来在促进东西方欧亚人群之间的迁徙和互动方面发挥了核心作用[2, 24, 73,74,75]。目前已提出三个重要假说来解释早期天山山脉人群的形成,包括内亚山地走廊(IAMC)内陆生物地理学假说、巴克特里亚绿洲假说和颜那亚/阿凡纳谢沃草原假说[73, 76]。然而,颅骨测量分析未能提供支持任何这些模型的有力证据[77]。来自准噶尔盆地(阿依托汗、松树沟和尼勒克)和塔里木盆地(古墓沟、百方和小河)地区的高质量全基因组数据代表了天山山脉发现的最早人类遗骸,为区域种群动态提供了新的见解。新疆南部早中青铜时代的塔里木人群是一个遗传隔离的群体,表现出高度的遗传亲缘性,但没有证据表明存在近亲关系[76]。对塔里木个体的遗传分析揭示了他们与两个古代东亚群体的联系:一个与古代东北亚(ANA)相关的贝加尔湖早青铜时代(Baikal_EB)人群有关,另一个以叶尼塞河上游地区旧石器时代晚期阿丰托瓦戈拉遗址(AG3)个体为代表(图 3)[76]。此外,遗传和牙结石蛋白质组学分析均表明,最早的塔里木盆地文化起源于本地隔离群体。这个最早的塔里木盆地群体可能从邻近的天山山脉人群那里采纳了畜牧和农耕实践,这与早期认为塔里木木乃伊(讲吐火罗语的游牧者)是来自阿凡纳谢沃、BMAC或内亚山地走廊文化的移民的理论形成了鲜明对比[73, 77]。
准噶尔群体呈现出与阿凡纳谢沃文化相关的遗传遗产,在青铜时代早期准噶尔个体中观察到大量阿凡纳谢沃文化的贡献和少量本地影响[76]。一项涵盖39个考古遗址201个古基因组的大规模古DNA研究聚焦于从青铜时代到历史时期的天山山脉相关人群,强调了塑造天山山脉地区人口历史的复杂且持续的混合事件[78]。Kumar等人报告称,天山山脉地区的青铜时代人群表现出高度的遗传多样性,并且与草原和东北亚人群存在区域遗传亲缘性。铁器时代加剧了天山山脉相关群体与草原和东北亚相关人群之间的混合。历史证据表明,自铁器时代以来,该地区与周边人群持续发生遗传混合并保持遗传连续性[72]。最近对塔里木西部24个青铜至铁器时代基因组的分析揭示了早期塔里木人群和迅速向西扩张的草原移民,这些群体首先与BMAC人群互动,随后与塔里木人群互动[79]。即使在铁器时代,本地祖源在整个塔里木盆地仍占主导地位,凸显了该地区复杂而迷人的历史。线粒体基因组数据进一步证实了与农业和畜牧人群的显著混合[78]。对距今约2200年的石人子沟遗址遗传多样个体的精细人口重建显示,东西方欧亚人之间的遗传交流影响了文化上同质的群体(图 4)[80]。此外,古DNA研究结果主要集中在阿尔泰和天山山脉的西部地区,而这些山脉东侧的数据有限。这种差异对于理解西方欧亚草原游牧者对东亚人群影响的边界至关重要。虽然颜那亚文化破坏了蒙古高原东部青铜时代的遗传结构,但西方欧亚遗传成分对不同时空河西走廊人群的贡献程度仍是古DNA研究中的一个关键问题。
古代蒙古高原人群的种群动态
与天山山脉相比,古代蒙古高原人群,特别是内蒙古人群的人口历史仍不明确,这主要是由于大规模古DNA数据的有限性。本综述通过分析零星地区报道的基因组以及蒙古高原北部邻近地区的数据,为种群历史提供了基本见解。来自蒙古高原东部(SOU001,eastMongolia_preBA)和北部(Fofonovo_EN)地区狩猎采集者的遗传特征表明,青铜时代之前蒙古高原的种群结构呈现出与古代东北亚祖源密切相关的遗传模式。这种模式与贝加尔湖西部距今7200-6200年的贝加尔湖早新石器时代(Baikal_EN)人群以及俄罗斯远东距今7700年的魔鬼洞新石器时代(DevilsCave_N)人群相似[81]。在青铜时代,蒙古高原的遗传结构呈现出三分格局,包括与北部库苏古尔湖晚青铜时代(Khovsgol_LBA)、西部阿尔泰山中晚青铜时代(Altai_MLBA)和东南部乌兰朱和-石板墓(Ulaanzuukh_SlabGrave)人群相关的不同乳制品畜牧群体。这种结构促进了混合遗传和文化模式的出现,这是由匈奴和其他历史游牧群体之间的互动驱动的[81, 82]。目前仅识别出一个距今8400年的新石器时代人群,即内蒙古乌兰察布的裕民人群。该人群与内陆新石器时代古代东北亚人群有遗传联系,并与古代东北亚相关的新石器时代西伯利亚人群和现代藏族人群有着密切的系统发育关系[54]。
最近的古基因组学研究证实,蒙古高原的种群历史以不同东西方欧亚人群之间的反复混合为特征[81]。历史文献记载,鲜卑作为蒙古高原地区一个重要的游牧民族,建立了北魏等政治王朝。Cai等人分析了9个距今约1800年的鲜卑个体的古基因组,揭示了与鲜卑人群南迁相关的遗传变化[83]。这一证据支持了鲜卑与黑龙江流域粟作农民或其后裔发生遗传混合的观点。此外,遗传数据表明,鲜卑在定居中国中原后,从游牧部落转变为定居农业者,并发生了显著的混合[83]。此外,Yang等人通过对距今约1300年的阿史那皇后古DNA的分析,追溯了突厥汗国的东北亚起源,并重建了北周王朝与突厥之间通过政治联姻形成的遗传联系[84]。中国武帝的古基因组表明其遗传起源与古代东北亚相关的鲜卑人群有关,并与汉族个体发生了额外混合[85]。最近使用现代基因组数据的混合分析也证实了汉族与北方游牧者之间的这种互动,以及更古老的长距离迁徙[67, 86]。来自时间校准系统发育树的Y染色体证据支持这样的假说,即武帝相关谱系和与生计相关的迁徙引入并促进了古代东北亚祖源的扩散[20, 87, 88]。然而,这也揭示了其对现代中国父系基因库的直接父系贡献有限。最近来自河西走廊和不同地理区域回族人群的历史和现代基因组也表明,西方欧亚影响渗透到了蒙古高原东部地区[24, 61, 89]。因此,阐明与西方草原游牧者的遗传互动至关重要,特别是考虑到内蒙古独特的地理位置。对长城内外古代基因组进行更广泛的分析对于更全面地理解种群动态至关重要。
古代东北亚人群的长期遗传稳定性
位于中国东北部的黑龙江流域和西辽河流域涵盖了广阔的山脉和平原,延伸至东部草原的一部分。这些地区的种群动态因其与美洲原住民和现代通古斯语族人群的密切遗传联系而备受关注[19]。Mao等人证明,中国北方的人类种群自距今约14000年以来一直保持着遗传连续性(图 3)[41]。基于qpWave/qpGraph模型推断的人口模式表明,来自魔鬼门和博伊斯曼的早期新石器时代个体,以及黑龙江流域的现代通古斯语族人群,表现出显著的基因组同质性[50]。Ning等人进一步证实了黑龙江流域上游地区早期新石器时代狩猎采集者和铁器时代人群的长期遗传稳定性[53]。来自后套木嘎遗址的未发表古基因组也支持这些初始人群对美洲原住民祖源的遗传连续性和显著贡献[90]。额外的种群遗传结构分析揭示了清晰的遗传分层,黑龙江流域新石器时代(AR_EN)和黑龙江流域鲜卑铁器时代(AR_Xianbei_IA)个体共享现代通古斯语族相关祖源。此外,在黑龙江流域铁器时代(AR_IA)个体中识别出可能的蒙古语族相关祖源,这支持了在现代阿尔泰语系人群形成过程中不同黑龙江流域人群之间存在基因流动的假说[53]。
位于黄河流域和黑龙江流域之间的西辽河流域在历史上经历了频繁的遗传转变,这反映了生计方式的变化。与古代黑龙江流域人群观察到的稳定遗传构成不同,古代西辽河流域人群的遗传组成在过去6000年中与生计方式的变化同步发生了显著波动[53]。Ning等人展示了中国北方与西辽河流域红山文化相关的半拉山古基因组,揭示了中晚新石器时代对粟作农业依赖的增加与和黄河流域粟作农民更强的遗传亲缘性相关[53]。Wang等人对19个红山文化郑家沟个体的基因组进行了测序,证实古代东北亚人群和与中新石器时代大汶口文化相关的农民促成了新石器时代红山人群的形成[91]。来自夏家店下层文化(二道井子晚新石器时代)的晚新石器时代群体也受到了类似的人群扩散模式的影响。相比之下,与青铜时代夏家店上层文化(龙头山青铜时代)相关的人群与黑龙江流域人群表现出更密切的遗传关系,这可能标志着他们转向以游牧业为主要生计方式[53]。Zhu等人在夏家店上层文化人群中识别出了独特的遗传亚结构,指出青铜时代晚期马家子山遗址的个体其祖源完全来自黄河流域粟作相关人群,这与龙头山青铜时代人群的遗传特征不同[92]。此外,青铜时代晚期的特点是欧亚草原上广泛的文化交流,导致西辽河流域和东部草原人群与西方欧亚遗传谱系发生混合[50, 66]。史前遗传变化进一步与长江流域稻作农业的强化实践相一致,表明生计方式转变可能驱动了人群扩散(图 4)[53, 66]。基于这些关联,Robbeets等人将中国北方新石器时代和青铜时代粟作农业的起源与汉藏语系和跨欧亚语系的出现联系起来。这些发现表明,语言和人群的扩散早在新石器时代晚期就已发生,主要是由粟作农民与大量古代东北亚、古代东北亚和西方欧亚祖源的逐渐混合驱动的[66]。
遗传学研究凸显了中国古代粟作农耕人群对周边区域的重要遗传贡献。例如,对朝鲜三国时期古代人群的谱系建模显示,其祖先谱系由青铜时代中国北方人群与绳文时代相关族群混合构成(图 4)[93]。罗贝茨等人解析了朝鲜、琉球群岛及早期谷物农耕社群的古基因组,证实东北亚首批农耕人群的迁徙活动留下了深远的遗传谱系印记[66]。同理,库克等人对比分析了日本农耕时代前后的古基因组,揭示绳文族群与大陆人群之间存在深远的遗传分化[94]。刘等人重建了山东地区古人群种群动态演化谱系,证实山东古代祖先谱系与日本列岛弥生时代之后人群的东亚大陆祖先谱系亲缘关系最近[95]。上述研究成果揭示了古东北亚祖先谱系与粟作农耕谱系的扩散路径,该过程推动了稻作与粟作农业向日本的传播;同时,东亚人群持续的基因交流重塑了日本人群基因组起源三元演化模型,并改变了其适应性生物演化格局[94, 96]。系列研究阐明了欧亚大陆古代人群之间深厚的历史亲缘关联,为厘清中国及周边跨欧亚区域的种群演化动态提供了理论依据。后续针对该区域人类演化史的研究,应优先获取具有代表性的古基因组序列,重点聚焦天山山脉东侧、蒙古高原东部及横断山区的早期农耕人群古DNA样本。此类研究将有助于更精细地阐释农业扩散进程及其对广袤地域语言、文化与人群适应性遗传基础的塑造机制。
青藏高原高地人群定居历程及其与新石器时代粟作农耕人群、藏彝走廊人群的遗传关联
青藏高原具有低压、低氧、低温及强紫外辐射等极端环境特征[97]。尽管生存环境严苛,藏族及其他高原世居族群及其祖先数千年来已演化出极强的高原环境适应能力[98]。目前学界仍存在若干关键科学问题尚未厘清:高原早期人群的始祖溯源、高原环境适应演化机制,具体涵盖遗传起源、高原特有祖先谱系、早期高原迁徙过程、永久定居时间节点,以及现代藏族人群基因库的形成演化脉络。布勒克洞穴遗址考古证据表明,丹尼索瓦人相关族群曾在海拔3280米的青藏高原东北部栖息,年代距今约16万至6万年[27]。尼雅德布狩猎采集人群约在距今3万至4万年前抵达青藏高原核心腹地(海拔4600米)[99]。青藏高原永久定居可能存在两条路径:其一为距今7400至12700年的曲桑狩猎采集人群,其二为后续由低地迁入、以大麦农业为生计的农耕族群[100, 101]。基于高覆盖全基因组测序及Y染色体、线粒体单亲遗传数据构建的复杂人口演化模型表明,旧石器时代人群定居与全新世人群扩张共同塑造了现代青藏高原高地人群的基因库构成[102, 103]。
青藏高原古人群的旧石器时代定居与新石器时代扩张
十年前,研究在现代藏族人群中检测到古老丹尼索瓦人型遗传组分,为解析青藏高原人群定居史提供了早期线索[33]。近年来大规模高地人群种群基因组研究产出的古基因组数据,进一步深化了学界对高原人群演化谱系的认知[104,105,106,107,108]。安纳普尔纳保护区古基因组样本(含乔霍帕尼遗址距今3150—2400年、梅布拉克遗址距今2400—1850年、萨姆宗遗址距今1750—1250年样本)验证了喜马拉雅古人群东亚高地起源假说,并证实该族群长期保持遗传结构稳定性[108]。距今约5100年的宗日遗址古基因组揭示了青藏高原特有遗传结构,其与古东北亚粟作农耕人群存在紧密遗传关联[106]。研究基于木斯塘、马南两地7处遗址(含苏拉、卢布拉克、里尔希、基昂等新遗址)共38例古基因组构建图谱演化模型,结果显示青藏高原古人群主体祖先谱系源自青藏高原东北部新石器时代晚期族群,同时少量承袭远古欧亚旧石器时代祖先组分[107]。该模型与学界既往提出的多波次迁徙塑造青藏高原定居史假说相互印证[60]。云南新石器时代兴义人群的最新研究,构建了目前与基底亚洲祖先谱系最直接的遗传关联;基底亚洲祖先曾被认为是高原人群谱系形成过程中关键的缺失古祖先源[48]。王等人开展大尺度时空分层基因组研究,发现距今2500余年青藏高原东、南、中、北各区域人群已呈现显著遗传分化。杨等人解析全球海拔最高定居聚落之一的马布措遗址古基因组[105]。对马布措湖域原生定居人群的基因组建模表明,该族群主体承袭高原南部祖先谱系[105]。系列研究同时证实青藏高原与东亚、东南亚人群间存在大规模基因交流,进一步塑造了现代藏族人群的遗传构成(图 3)[105, 106]。白等人针对阿里地区古代藏西人群开展精细遗传建模,解析其种群动态演化规律[104]。研究发现藏西人群保持长达3500年的区域遗传连续性,存在多次高原族群南向向西扩张事件,且古格王朝人群与中亚、南亚族群间存在基因交流[104]。此外,青藏高原历史时期人群与欧亚大陆其他族群存在广泛遗传交融。朱等人报道都兰遗址10例吐蕃相关古样本(距今1308—1130年),证实吐蕃帝国通过人口迁徙与文化扩散双重路径影响青藏高原东北部,并在历史时期作用于藏族核心族群及欧亚草原相关祖先谱系人群[109]。
藏彝走廊古人群的中国北方起源
青藏高原东北部历来是人群迁入高原的关键廊道;宗日、喇家、金禅口等遗址古基因组证实,粟作农耕人群与高原人群间存在密切遗传亲缘关系。刘等人识别出藏缅语族中海拔聚居人群独特的遗传演化脉络,该区域位于青藏高原东南缘与东缘,是藏彝走廊的重要地理通道之一[107]。藏彝走廊作为南北迁徙平行廊道之一,承担着西南地区藏缅语族人群向东南亚低地扩散的地理枢纽功能[107]。该区域地处青藏高原东缘,地理环境格局复杂。黄河流域广泛分布源自中国北方的粟作相关祖先谱系,而现今栖息于藏彝走廊的藏缅语族人群呈现显著遗传分化,大概率源于选择压力差异与适应性遗传性状的演化分异[22]。古DNA技术的突破性进展,为厘清史前时代农业传播、文化扩散及人群迁徙演化轨迹提供了新途径[110, 111]。陶等人报道中国西南新石器时代高山遗址与青铜时代海门口遗址全基因组数据,两处遗址距今4500—3000年同时存续粟作与稻作混合农业生计模式[111]。新石器时代高山与海门口人群约90%的祖先谱系源自黄河流域粟作农耕人群,同时保留狩猎采集人群遗传支系,未检测到稻作农耕人群遗传组分。该结果表明,藏彝走廊粟作农耕人群在接纳稻作农业生产方式的过程中,未发生显著遗传同化,佐证了区域农业传统独立演化的学术观点[111]。此外,青藏高原东北坡及雅鲁藏布江流域检出的古人群,与藏彝走廊古人群遗传亲缘关系显著,提示两条迁徙廊道共同塑造了二者共享的遗传基底(图 2)。四川眉山4处古代崖墓人群基因组数据,同样证实其与古东北亚农耕人群遗传关联紧密[112]。综上,古基因组学证据一致支撑:现代与古代藏彝走廊人群及藏缅语族人群,均起源于中国北方粟作农耕族群。
多学科交叉证据(尤其是考古学与古DNA研究新进展)已系统厘清青藏高原人类定居演化史。考古遗存记录了青藏高原悠久的人类活动史,代表性遗址包括布勒克洞穴遗址[28]、尼雅德布遗址[85]与曲桑遗址[100, 101]。中国西北地区最早古DNA样本出自距今约5100年的宗日遗址狩猎采集人群[106]。但仅依靠现有遗传数据的时间跨度,尚不足以精准界定人类初始定居青藏高原的年代。同时,仍需扩充藏彝走廊人群跨时空古DNA采样,以厘清青藏高原古人群与藏彝走廊早期定居者的遗传亲缘关系及谱系分化时间。
东亚人群古代生物适应性演化研究
古DNA在追溯人类疾病遗传起源中的研究价值
人类疾病与复杂性状的演化驱动机制受多重因素共同塑造,包括青藏高原极端环境胁迫、病原体暴露(如中国南方疟疾流行)及史前生计模式转型等。既往研究主要依托基因组变异图谱,结合高级统计与计算推演解析上述演化决定因素[113]。具备全域时空覆盖度的古遗传分析,可直接揭示既往未知的人群演化动态与人类疾病易感谱系的内在关联,阐释适应性遗传特征的演化根基,并解析现代环境下疾病发生的演化成因[114,115,116,117]。古DNA通过解析远古环境下有利遗传变异对现代人类健康与疾病易感性的塑造作用,同时将演化理论应用于疾病风险预测与临床诊疗,为演化医学研究提供了重要数据支撑。
学界已通过追溯祖先基因交流脉络,解析健康相关性状的演化塑造机制;相关遗传研究已聚焦现代及古代欧洲人群多发性硬化症的潜在遗传起源[114]。古DNA在人类疾病研究中的另一重要价值,是依托时空演化窗口验证经典演化假说,包括节俭基因假说、卫生假说、拮抗多效性假说等[115, 118]。利用古DNA时序序列特征,可追溯远古适应性遗传演化轨迹,识别不同环境压力下关乎种群存续的关键遗传变异,涵盖疾病抗性、饮食耐受及气候胁迫适应等维度。阿克巴里等人检出乳糜泻、B型血型相关疾病、肺结核易感、类风湿关节炎及其他31类经古DNA验证、受定向选择作用的疾病性状,获得全基因组显著演化信号与强定向选择印记[115]。大尺度古DNA研究同时揭示了重塑人类数十类复杂性状与疾病的多层级定向选择机制。此类研究有助于解析糖尿病、心血管疾病、肿瘤等复杂慢病的演化成因,此类疾病多受祖先基因交流驱动演化。
古DNA技术也实现了对古人群遗传谱系遗产的精准解析,阐明祖先基因交流如何塑造现代人类基因库中复杂疾病性状的遗传架构[119]。马内托等人整合古代与现代欧洲人群基因组混合演化模型,区分出贡献于人体测量性状、色素沉着特征与代谢性状分化的古欧洲祖先源;例如本地狩猎采集谱系与亚姆纳亚草原祖先谱系对胆固醇水平存在差异化调控效应[119]。此外,远古人类迁徙过程中渗入的基因组分(含早期智人、尼安德特人基因渐渗),进一步厘清了人类疾病易感与抗性特征的遗传底层机制[6,7,8]。以尼安德特人基因渐渗为例,其与人类抗感染免疫应答调控密切相关。
古DNA已完整记录全新世数千年间农业革命引发的遗传变异,重点涵盖免疫相关宿主—病原体共演化、慢性疾病、衰老进程及代谢紊乱相关遗传改变[114, 116, 118]。研究证实,疾病易感相关遗传变异处于持续演化状态;远古病原体抗性变异至今仍深刻影响现代人群疾病易感性。通过解析此类变异,演化医学可明确调控当代健康与疾病发生的分子通路。克尔纳等人近期研究表明,全新世宿主—病原体互作格局推动了人群传染病适应性演化,同时也调控着炎症性疾病的易感谱系[116]。
古DNA与现代基因组数据的整合研究,完善了人类演化及其健康效应的整体理论框架。若古人群携带赋予人类疾病抗性的免疫相关遗传变异,通过与携带同源变异的现代人群对比,可阐明该类性状对当代疾病预后的调控机制[116]。该研究范式可为精准医学与遗传咨询提供理论支撑。巴里等人结合南欧、北欧现代人群多发性硬化症患病风险与古人类迁徙、人群混合年代开展关联分析[114]。结果发现,多发性硬化症遗传易感风险升高与草原游牧人群祖先谱系存在强关联。但近期大规模古今欧洲人群基因组分析显示,北欧人群多发性硬化症高易感风险并非由草原游牧人群选择压力所致;尽管距今约6000至2000年间,HLA-DRB1*15:01位点正向选择频率已升至18%[115]。
基于古DNA解析东亚人群演化轨迹
东亚古DNA资源为解析当代健康相关性状的演化起源提供了独特研究载体,有望推动疾病预防策略、精准个体化医学发展,并深化遗传易感体质的形成机制认知[114,115,116,117,118,119]。祖先基因交流的演化脉络结合古DNA解析成果,进一步丰富了人类健康与疾病的遗传底层理论。目前中国古DNA样本存量不足,制约了东亚人群特有性状演化驱动机制的系统性阐释(图 5—6)。库马尔等人解析天山山脉人群祖先谱系更替引发的表型分化,证实天山中西部人群自青铜时代晚期至铁器时代,毛发与肤色色素沉着持续变浅;铁器时代该区域已出现蓝眼等位基因。值得注意的是,全部5例历史时期古样本均表现为深色虹膜与毛发色素特征,反映该阶段人群东亚、南亚、中亚祖先谱系成分占比提升[72]。
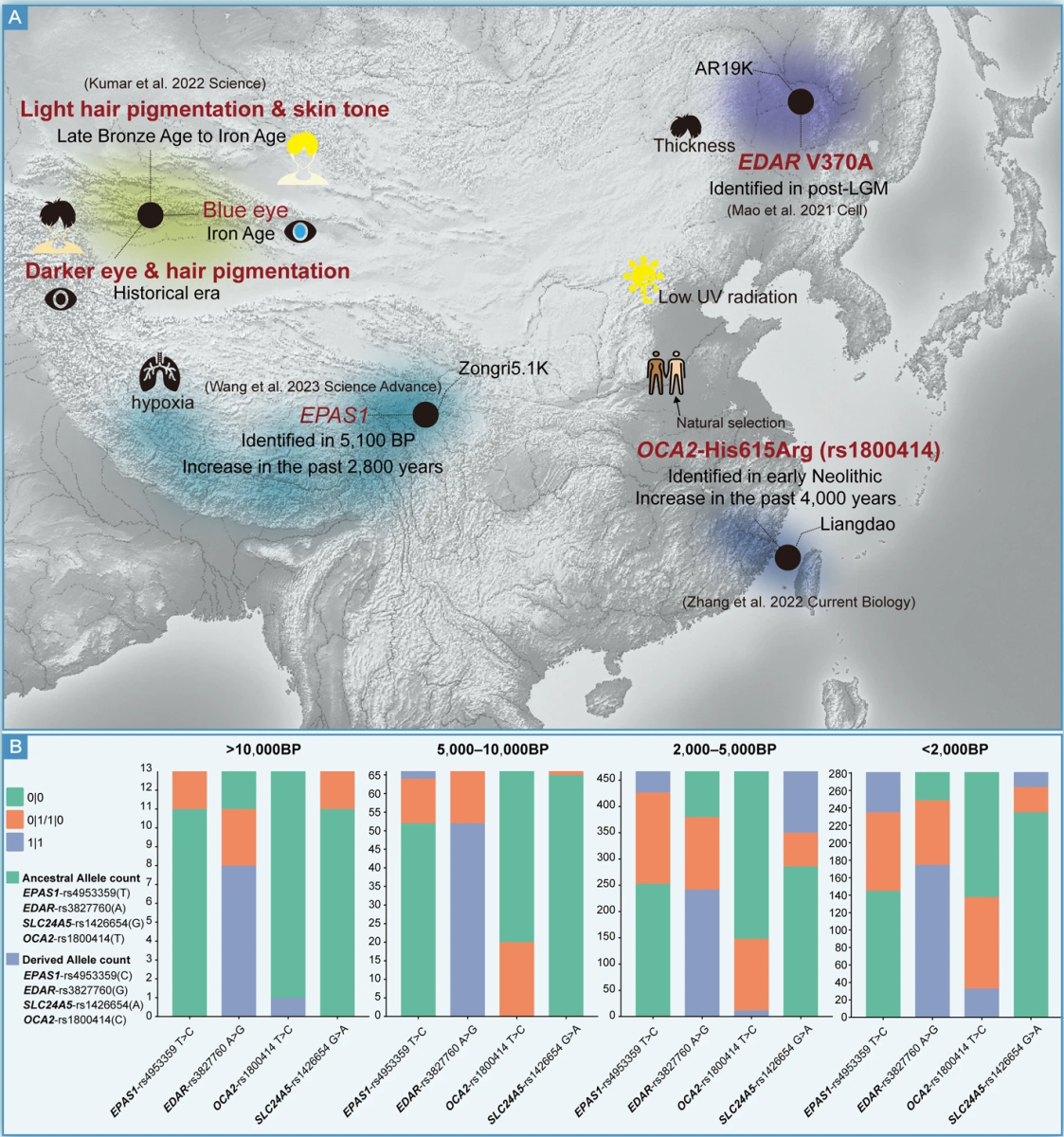
为解析东亚人群特有EDAR V370A遗传变异的演化轨迹(该变异调控毛发直径加粗等表型特征),毛等人整合25例古东北亚人群全基因组数据及已发表田园洞古人群数据,时间跨度涵盖末次冰盛期前后(距今4万至6千年),提供了关键演化证据(图 5)。研究发现,末次冰盛期之后所有东亚古人群均携带V370A突变,提示该变异在末次冰盛期期间或冰盛期后不久开始广泛扩散(图 5)[41]。另一项研究中,张等人将OCA2-His615Arg(rs1800414)变异的起源追溯至中国华南沿海岛屿新石器时代早期。该变异在过去4000年间频率显著上升,推测受达尔文正向选择作用驱动;该选择效应或推动高纬度人群肤色变浅,以适应高纬度地区紫外辐射偏弱的环境特征(图 5)[43]。
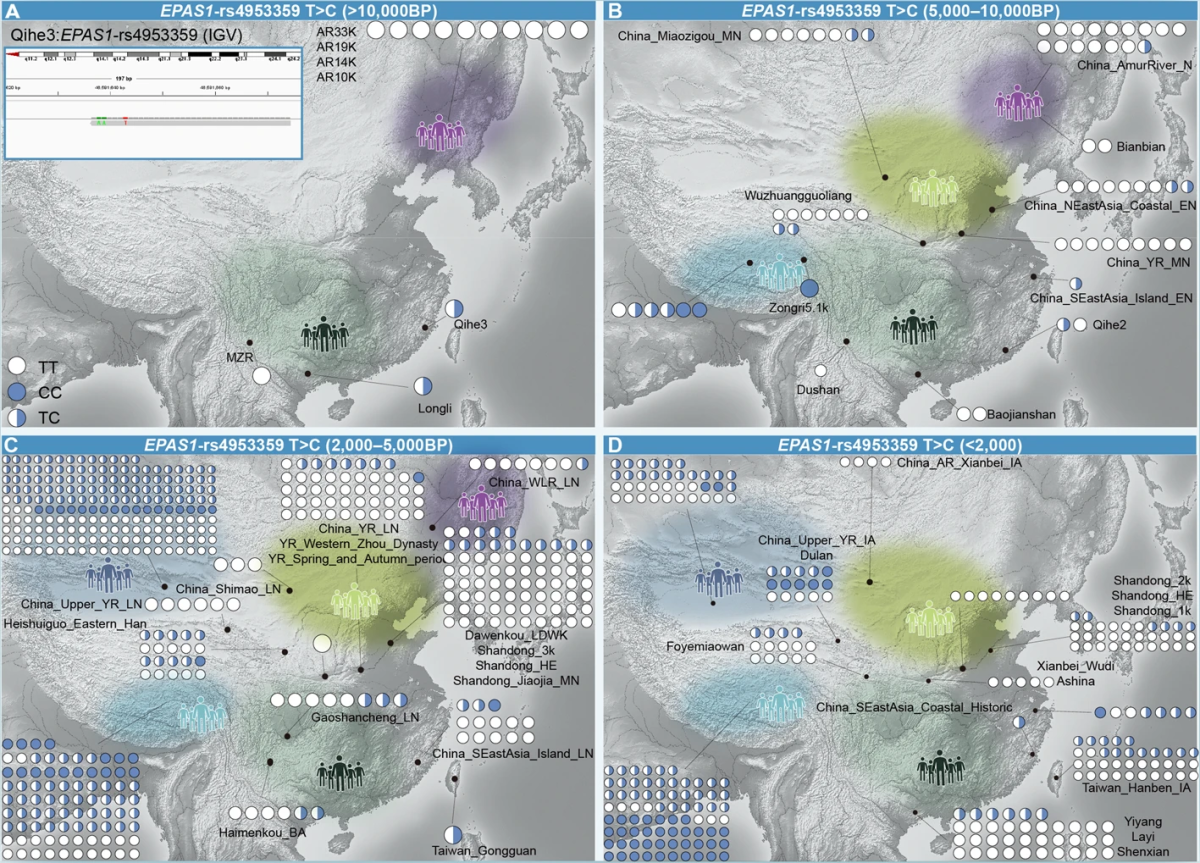
基因渐渗可将古老人属种群的遗传变异导入现代人群,并接受自然选择筛选,为解析人类表型分化与适应性性状的遗传调控机制提供重要线索[120]。调控高原适应能力的EPAS1基因,已在距今5100年青藏高原古个体及新近发表的大地湾古人群样本中检出,且该变异频率在过去2800年间持续攀升(图 6)。此外,高等人基于36个中国人群泛基因组数据证实,中国人群特有的古老基因渐渗等位基因与角质形成、紫外应答、DNA修复、免疫功能及寿命调控等功能性状显著关联[121]。现代人群大尺度基因组数据同时提示,东亚人群特有适应性性状(如酒精代谢相关ADH/ALDH基因、农耕饮食相关MTHFR基因)的演化轨迹,仍需古DNA证据进一步佐证。对人类表型变异相关遗传变异开展时空溯源,可厘清史前遗传多样性格局,阐释自然选择对生物适应性演化时序的调控规律。受限于中国古DNA样本储量不足,适应性变异的起源年代、选择作用启动节点及复杂性状精细演化轨迹目前仍无法精准界定。随着古DNA数据持续积累,未来有望实现更精准的年代估算与更高分辨率的时空演化溯源[43]。
研究挑战与未来展望
人类复杂性状遗传架构的演化基础
古基因组数据为人类局部适应性演化以及健康与疾病的遗传底层机制研究提供了关键依据[122]。该领域研究进展的典型案例是,学界已识别出源自尼安德特人的遗传风险因子,该因子会提升新冠肺炎重症感染的易感风险[123]。欧洲新石器时代之后的自然选择印记表明,人群针对病原体的遗传适应性演化重塑了免疫相关基因,并升高了炎症性疾病的发病风险[116]。马内托等人研究指出,大麦农耕人群、草原游牧人群与欧洲本地狩猎采集人群的祖先组分,共同构成了现代欧洲人群复杂性状的遗传变异基础[119]。中国近年古DNA研究进一步完善了区域适应性演化轨迹的认知,明确了EPAS1等关键遗传标记与青藏高原极端环境适应的关联[106];同时也证实已被广泛研究的EDAR V370A变异对中原地区人群形态性状具有调控作用[41]。此外,遗传学证据显示,西欧亚人群东迁对天山区域古代人群的色素沉着性状产生了显著影响[72]。但目前中国古DNA数据仍存在时空覆盖范围不足的短板,制约了从演化视角系统阐释人类健康与疾病遗传机制的研究进程。沉积物DNA分析、古蛋白质组学、同位素分析、微生物组研究及表观遗传图谱解析等新兴技术方法,配合专为古DNA分析开发的生物信息学工具,有望深化学界对远古人群健康特征以及遗传因素在人类演化中作用机制的认知[1, 124,125,126]。依托多组学技术对古人类遗存与沉积物样本开展研究,可为古今人类演化及其与微生物协同演化机制提供全新学术视角。
高质量人群特异性古基因组数据库与单倍型参考面板
古DNA提取、古人类遗存测序技术与古DNA分型及基因型填充技术的融合应用,仍存在较大技术创新空间[114, 127]。受古生物死后DNA降解与污染干扰,低测序深度古基因组的基因型精准判读仍面临瓶颈。在此背景下,依托具有祖先谱系代表性的现代人群构建人群特异性高质量单倍型参考面板,开展古基因组基因型填充,已成为提升低覆盖度古DNA基因分型准确度的可靠技术路径[128]。古DNA数据存量快速增长预示着未来将涌现更多祖先谱系多元、时空维度丰富的古基因组资源,亟需构建适配东亚人群的专属单倍型参考面板,并建立统一公认的基因型填充技术规范[128, 129]。当前多数古DNA研究仅基于单核苷酸多态性共享模式开展分析,缺乏依托单倍型数据解析精细人群遗传结构的研究范式。亟需建立模拟验证基准体系,加快研发适配古DNA分析的人群特异性单倍型参考面板、单倍型分型与填充软件及专属数据库,填补现有研究短板[130]。
多学科协同研究与原住民社群参与的必要性
跨学科协作与高效学术沟通,是构建古DNA研究均衡学术叙事体系的核心前提[131]。考古学、遗传学、人类学及动植物科学领域学者的跨界合作,极大推动了古DNA学科发展。整合农业起源中心及其周边区域古代驯化动植物的起源、适应性演化与生物性状变异研究成果,能够更系统阐释人类迁徙与生物演化的复杂动态过程[46, 132, 133]。另一方面,古DNA研究与法医遗传学共同面临降解样本DNA分型提取的技术难题。奇尔德巴耶娃等人梳理了低覆盖度二代测序数据的分析计算流程,明确各研究环节的技术局限与决策规范,对古DNA与法医遗传学领域的发展具有重要支撑作用[134]。法医遗传学侧重从碎片化物证中提取DNA信息并关联特定个体,结合表型特征、遗传祖先溯源与亲缘关系溯源缩小侦查范围[134]。与之不同,古DNA研究以古代人类遗存为研究材料(多采用捕获测序技术),旨在解析史前人群种群互动模式[53, 72, 111]、验证人群迁徙演化假说[54, 66, 76]、厘清古今人群间遗传亲缘关系[1, 4, 41, 42, 50, 106]。鉴于两大领域应用场景的差异,亟需针对中国人群开展古DNA与法医遗传学研究的系统性验证,保障研究实际应用价值。同时需融合遗传学、基因组学、考古学、民族学与语言学多学科理论,提升古DNA研究的深度与完整性。
古代社会发展与家族谱系的精细重建
古DNA技术的突破性进展,彻底革新了学界对史前文化变迁与复杂社会组织形态的认知[131]。依托古DNA研究,学界对史前社会家族结构的生物学内涵形成了更为精准的解读[135]。多项核心古DNA研究通过解析合葬遗存人群的遗传亲缘关系,成功重建古代复杂社会结构,揭示了史前人类社会多维度特征;相关成果阐明了旧石器时代狩猎采集人群的社会行为与繁衍模式、安纳托利亚新石器时代人群多元亲属制度,以及青铜时代游牧族群的谱系传承、婚姻形态与聚落居住格局[135,136,137]。傅家遗址与八里岗遗址两项古DNA研究,初步探讨了母系与父系社群结构对黄河流域及长江流域新石器时代人群社会组织形态的塑造作用[62, 138]。整合不同历史时期文化传统、婚姻习俗与丧葬制度特征,构建东亚古代社会组织形态完整谱系,是还原东亚人群演化全貌并解析其驱动因素的必要路径[112]。
结论
本研究系统梳理了东亚分化深远的狩猎采集人群祖先谱系演化史,涵盖古东亚北方祖先人群、隆林人群、淇河人群与芒孜人群,分别对应古北方祖先谱系、广西本地谱系、福建谱系与云南谱系。同时全面阐释了全新世东欧亚人群种群动态演化规律,重点聚焦粟作农耕人群、稻作农耕人群与游牧人群,证实复杂的人群迁徙与遗传混合过程塑造了古今东亚人群的基因组多样性。中原地区(尤以黄河流域为核心)被认定为汉藏语系起源地与早期农业文明中心;该区域狩猎采集人群与农耕人群,联合长江流域稻作农耕人群,共同构成了东亚其他区域人群的主体祖先谱系。湿热环境下古DNA保存难度大的技术瓶颈,制约了中国长江中下游稻作农耕人群关键时空序列样本的获取。全新世东亚不同地理单元古基因组资源相对匮乏,亟需构建高质量、高覆盖度、时空分辨率完备的古基因组数据库。该数据库将助力阐释旧石器时代狩猎采集人群、新石器时代农耕人群、青铜时代游牧人群及现代东亚人群的疾病演化起源与生物适应性演化机制。尽管东亚古DNA研究已完善了东欧亚大陆人类演化史框架,但古DNA数据仍存在时空断层,难以完整厘清稻作与粟作农耕人群及其先祖、后裔的遗传谱系特征。构建时空高覆盖度的完整古基因组数据集,是阐明东亚人群起源与演化轨迹的关键基础。
材料与方法
本文详细研究方法见补充文件1。本研究整合古人类基因组资源数据库与近年已发表的东亚古今人群DNA数据,最终构建包含929个个体的分析数据集[3, 26, 42, 43, 50, 53, 80, 106, 111, 139,140,141]。基于连锁不平衡精简后的单核苷酸多态性位点,采用ADMIXTURE v1.3.0软件开展祖先成分分析,识别四类核心祖先谱系源,并在K=6聚类水平下区分地理分异人群[142, 143]。依托EIGENSOFT软件内置smartpca算法开展主成分分析,实现古今人群聚类,解析东亚全域遗传亚结构特征。对古个体BAM测序文件进行处理,评估古DNA死后降解损伤特征[41,42,43, 50, 53,54,55,56, 58, 61, 64, 72, 76, 80, 84, 85, 92, 104, 106, 109, 111, 145,146,147,148];依托人群特异性参考面板,采用GLIMPSE2软件完成基因型填充[127, 128]。本研究执行严格质控流程,保障高分辨率基因组分析精度,深化了东亚人群演化史的科学认知。
数据可用性
本研究所有数据与分析代码均已上传至Zenodo学术数据平台。资源库包含本研究生成的填充后古基因组数据集、所分析古基因组的详细信息与参考文献,以及数据处理与分析专用脚本。填充后古基因组数据访问地址:https://zenodo.org/records/17270846[149];分析代码与详细研究资料访问地址:https://zenodo.org/records/17270850[150];主成分分析、祖先成分分析等可视化代码访问地址:https://doi.org/10.5281/zenodo.17271668[151]。本研究其余所有衍生数据均已收录于正文及补充文件中。
参考文献
- Liu Y, Mao X, Krause J, Fu Q. Insights into human history from the first decade of ancient human genomics. Science. 2021;373:1479–84.
- He G, Wang M, Luo L, Sun Q, Yuan H, Lv H, et al. Population genomics of Central Asian peoples unveil ancient trans-Eurasian genetic admixture and cultural exchanges. hLife. 2024;2:554–62.
- Bergstrom A, McCarthy SA, Hui R, Almarri MA, Ayub Q, Danecek P, Chen Y, Felkel S, Hallast P, Kamm J, et al: Insights into human genetic variation and population history from 929 diverse genomes. Science. 2020;367.
- Avila-Arcos MC, Raghavan M, Schlebusch C. Going local with ancient DNA: a review of human histories from regional perspectives. Science. 2023;382:53–8.
- Racimo F, Sikora M, Vander Linden M, Schroeder H, Lalueza-Fox C. Beyond broad strokes: sociocultural insights from the study of ancient genomes. Nat Rev Genet. 2020;21:355–66.
- Zeberg H, Jakobsson M, Paabo S. The genetic changes that shaped Neandertals, Denisovans, and modern humans. Cell. 2024;187:1047–58.
- Peyregne S, Slon V, Kelso J. More than a decade of genetic research on the Denisovans. Nat Rev Genet. 2024;25:83–103.
- Ongaro L, Huerta-Sanchez E. A history of multiple Denisovan introgression events in modern humans. Nat Genet. 2024;56:2612–22.
- Reich D, Green RE, Kircher M, Krause J, Patterson N, Durand EY, et al. Genetic history of an archaic hominin group from Denisova Cave in Siberia. Nature. 2010;468:1053–60.
- Green RE, Krause J, Briggs AW, Maricic T, Stenzel U, Kircher M, et al. A draft sequence of the Neandertal genome. Science. 2010;328:710–22.
- Prufer K, de Filippo C, Grote S, Mafessoni F, Korlevic P, Hajdinjak M, et al. A high-coverage Neandertal genome from Vindija Cave in Croatia. Science. 2017;358:655–8.
- Mafessoni F, Grote S, de Filippo C, Slon V, Kolobova KA, Viola B, et al. A high-coverage Neandertal genome from Chagyrskaya Cave. Proc Natl Acad Sci U S A. 2020;117:15132–6.
- Prufer K, Racimo F, Patterson N, Jay F, Sankararaman S, Sawyer S, et al. The complete genome sequence of a Neanderthal from the Altai Mountains. Nature. 2014;505:43–9.
- Larena M, McKenna J, Sanchez-Quinto F, Bernhardsson C, Ebeo C, Reyes R, et al. Philippine Ayta possess the highest level of Denisovan ancestry in the world. Curr Biol. 2021;31(4219–4230):e4210.
- Choin J, Mendoza-Revilla J, Arauna LR, Cuadros-Espinoza S, Cassar O, Larena M, et al. Genomic insights into population history and biological adaptation in Oceania. Nature. 2021;592:583–9.
- Stoneking M, Arias L, Liu D, Oliveira S, Pugach I, Rodriguez J. Genomic perspectives on human dispersals during the Holocene. Proc Natl Acad Sci U S A. 2023;120:e2209475119.
- de Barros Damgaard P, Martiniano R, Kamm J, Moreno-Mayar JV, Kroonen G, Peyrot M, Barjamovic G, Rasmussen S, Zacho C, Baimukhanov N, et al: The first horse herders and the impact of early Bronze Age steppe expansions into Asia. Science. 2018;360.
- Sikora M, Pitulko VV, Sousa VC, Allentoft ME, Vinner L, Rasmussen S, et al. The population history of northeastern Siberia since the Pleistocene. Nature. 2019;570:182–8.
- Raghavan M, Steinrucken M, Harris K, Schiffels S, Rasmussen S, DeGiorgio M, et al. Genomic evidence for the Pleistocene and recent population history of Native Americans. Science. 2015;349:aab3884.
- Wang M, Sun Q, Feng Y, Wei LH, Liu K, Luo L, et al. Paleolithic divergence and multiple Neolithic expansions of ancestral nomadic emperor-related paternal lineages. J Genet Genomics. 2025;52:502–12.
- Wang M, Chen H, Luo L, Huang Y, Duan S, Yuan H, et al. Forensic investigative genetic genealogy: expanding pedigree tracing and genetic inquiry in the genomic era. J Genet Genomics. 2025;52:460–72.
- Sun Y, Wang M, Sun Q, Liu Y, Duan S, Wang Z, et al. Distinguished biological adaptation architecture aggravated population differentiation of Tibeto-Burman-speaking people. J Genet Genomics. 2024;51:517–30.
- Luo L, Wang M, Liu Y, Li J, Bu F, Yuan H, et al. Sequencing and characterizing human mitochondrial genomes in the biobank-based genomic research paradigm. Sci China Life Sci. 2025;68:1610–25.
- He G, Yao H, Duan S, Luo L, Sun Q, Tang R, et al. Pilot work of the 10K Chinese people genomic diversity project along the Silk Road suggests a complex east-west admixture landscape and biological adaptations. Sci China Life Sci. 2025;68:914–33.
- Deng S, Chen F. Trends in ancient human genomics research. Chinese Science Bulletin-Chinese. 2023;68:2544–9.
- Mallick S, Micco A, Mah M, Ringbauer H, Lazaridis I, Olalde I, et al. The Allen Ancient DNA Resource (AADR) a curated compendium of ancient human genomes. Sci Data. 2024;11:182.
- Chen F, Welker F, Shen CC, Bailey SE, Bergmann I, Davis S, et al. A late middle Pleistocene Denisovan mandible from the Tibetan Plateau. Nature. 2019;569:409–12.
- Zhang D, Xia H, Chen F, Li B, Slon V, Cheng T, et al. Denisovan DNA in late Pleistocene sediments from Baishiya Karst Cave on the Tibetan Plateau. Science. 2020;370:584–7.
- Fu Q, Bai F, Rao H, Chen S, Ji Y, Liu A, et al. The proteome of the late middle Pleistocene Harbin individual. Science. 2025;389:704–7.
- Fu Q, Cao P, Dai Q, Bennett EA, Feng X, Yang MA, et al. Denisovan mitochondrial DNA from dental calculus of the >146,000-year-old Harbin cranium. Cell. 2025;188(3919–3926):e3919.
- Racimo F, Sankararaman S, Nielsen R, Huerta-Sanchez E. Evidence for archaic adaptive introgression in humans. Nat Rev Genet. 2015;16:359–71.
- Zhang X, Witt KE, Banuelos MM, Ko A, Yuan K, Xu S, et al. The history and evolution of the Denisovan-EPAS1 haplotype in Tibetans. Proc Natl Acad Sci U S A. 2021;118:e2020803118.
- Huerta-Sanchez E, Jin X, Asan, Bianba Z, Peter BM, Vinckenbosch N, Liang Y, Yi X, He M, Somel M, et al: Altitude adaptation in Tibetans caused by introgression of Denisovan-like DNA. Nature. 2014;512:194–197.
- Feng X, Yin Q, Gao F, Lu D, Fang Q, Feng Y, et al. The phylogenetic position of the Yunxian cranium elucidates the origin of Homo longi and the Denisovans. Science. 2025;389:1320–4.
- Fu Q, Posth C, Hajdinjak M, Petr M, Mallick S, Fernandes D, et al. The genetic history of Ice Age Europe. Nature. 2016;534:200–5.
- Shang H, Tong H, Zhang S, Chen F, Trinkaus E. An early modern human from Tianyuan Cave, Zhoukoudian, China. Proc Natl Acad Sci U S A. 2007;104:6573–8.
- Kuhlwilm M, Gronau I, Hubisz MJ, de Filippo C, Prado-Martinez J, Kircher M, et al. Ancient gene flow from early modern humans into eastern Neanderthals. Nature. 2016;530:429–33.
- Fu Q, Meyer M, Gao X, Stenzel U, Burbano HA, Kelso J, et al. DNA analysis of an early modern human from Tianyuan Cave, China. Proc Natl Acad Sci USA. 2013;110:2223–7.
- Yang MA, Gao X, Theunert C, Tong H, Aximu-Petri A, Nickel B, et al. 40,000-Year-Old Individual from Asia Provides Insight into Early Population Structure in Eurasia. Curr Biol. 2017;27(3202–3208):e3209.
- Raghavan M, Skoglund P, Graf KE, Metspalu M, Albrechtsen A, Moltke I, et al. Upper Palaeolithic Siberian genome reveals dual ancestry of Native Americans. Nature. 2014;505:87–91.
- Mao X, Zhang H, Qiao S, Liu Y, Chang F, Xie P, et al. The deep population history of northern East Asia from the Late Pleistocene to the Holocene. Cell. 2021;184(3256–3266):e3213.
- Wang T, Wang W, Xie G, Li Z, Fan X, Yang Q, et al. Human population history at the crossroads of East and Southeast Asia since 11,000 years ago. Cell. 2021;184(3829–3841):e3821.
- Zhang X, Ji X, Li C, Yang T, Huang J, Zhao Y, et al. A Late Pleistocene human genome from Southwest China. Curr Biol. 2022;32(3095–3109):e3095.
- Lipson M, Cheronet O, Mallick S, Rohland N, Oxenham M, Pietrusewsky M, et al. Ancient genomes document multiple waves of migration in Southeast Asian prehistory. Science. 2018;361:92–5.
- Yang X, Wan Z, Perry L, Lu H, Wang Q, Zhao C, et al. Early millet use in northern China. Proc Natl Acad Sci USA. 2012;109:3726–30.
- Ma T, Rolett BV, Zheng Z, Zong Y. Holocene coastal evolution preceded the expansion of paddy field rice farming. Proc Natl Acad Sci USA. 2020;117:24138–43.
- Xiong J, Xu Y, Chen G, Yang L, Zhou Y, Pan Y, Wang Z, Bai J, Zhang B, Dong G, et al: The genomic history of East Asian Middle Neolithic millet- and rice-agricultural populations. Cell Genom. 2025:100976.
- Wang T, Yang MA, Zhu Z, Ma M, Shi H, Speidel L, et al. Prehistoric genomes from Yunnan reveal ancestry related to Tibetans and Austroasiatic speakers. Science. 2025;388:eadq9792.
- Zhang M, Yan S, Pan W, Jin L. Phylogenetic evidence for Sino-Tibetan origin in northern China in the late Neolithic. Nature. 2019;569:112–5.
- Wang CC, Yeh HY, Popov AN, Zhang HQ, Matsumura H, Sirak K, et al. Genomic insights into the formation of human populations in East Asia. Nature. 2021;591:413–9.
- Sagart L, Jacques G, Lai Y, Ryder RJ, Thouzeau V, Greenhill SJ, et al. Dated language phylogenies shed light on the ancestry of Sino-Tibetan. Proc Natl Acad Sci USA. 2019;116:10317–22.
- Lazaridis I, Nadel D, Rollefson G, Merrett DC, Rohland N, Mallick S, et al. Genomic insights into the origin of farming in the ancient Near East. Nature. 2016;536:419–24.
- Ning C, Li T, Wang K, Zhang F, Li T, Wu X, et al. Ancient genomes from northern China suggest links between subsistence changes and human migration. Nat Commun. 2020;11:2700.
- Yang MA, Fan X, Sun B, Chen C, Lang J, Ko YC, et al. Ancient DNA indicates human population shifts and admixture in northern and southern China. Science. 2020;369:282–8.
- Du P, Zhu K, Wang M, Sun Z, Tan J, Sun B, et al. Genomic dynamics of the Lower Yellow River Valley since the Early Neolithic. Curr Biol. 2024;34(3996–4006):e3911.
- Li S, Wang R, Ma H, Tu Z, Qiu L, Chen H, et al. Ancient genomic time transect unravels the population dynamics of Neolithic middle Yellow River farmers. Sci Bull. 2024;69:3365–70.
- Ma H, Zhou Y, Wang R, Yan F, Chen H, Qiu L, et al. Ancient genomes shed light on the long-term genetic stability in the Central Plain of China. Sci Bull. 2025;70:333–7.
- Wang F, Wang R, Ma H, Zeng W, Zhao Y, Wu H, et al. Neolithization of Dawenkou culture in the lower Yellow River involved the demic diffusion from the Central Plain. Sci Bull. 2024;69:3677–81.
- He GL, Wang MG, Li YX, Zou X, Yeh HY, Tang RK, et al. Fine-scale north-to-south genetic admixture profile in Shaanxi Han Chinese revealed by genome-wide demographic history reconstruction. J Syst Evol. 2021;60:955–72.
- He G, Wang M, Zou X, Chen P, Wang Z, Liu Y, et al. Peopling history of the Tibetan Plateau and multiple waves of admixture of Tibetans inferred from both ancient and modern genome-wide data. Front Genet. 2021;12:725243.
- Xiong J, Wang R, Chen G, Yang Y, Du P, Meng H, et al. Inferring the demographic history of Hexi Corridor over the past two millennia from ancient genomes. Sci Bull. 2024;69:606–11.
- Yang T, He J, Li C, Ning C, Zhang T, Wang J, et al. Ancient DNA reveals the population interactions and a neolithic patrilineal community in Northern Yangtze Region. Nat Commun. 2025;16:8728.
- Matsumura H, Hung HC, Higham C, Zhang C, Yamagata M, Nguyen LC, et al. Craniometrics Reveal “Two Layers” of Prehistoric Human Dispersal in Eastern Eurasia. Sci Rep. 2019;9:1451.
- Zhang F, Zhang XL, Bai B, Hu CG, Duan C, Yuan HB, Zhang RJ, Ma PC, Zhou BS, Ning C: Ancient genomes provide insights into the genetic history in the historical era of southwest China. Archaeological and Anthropological Sciences. 2024;16.
- Zhu K, Hu C, Yang M, Zhang X, Guo J, Xie M, et al. The demic diffusion of Han culture into the Yunnan-Guizhou plateau inferred from ancient genomes. Natl Sci Rev. 2024;11:nwae387.
- Robbeets M, Bouckaert R, Conte M, Savelyev A, Li T, An DI, et al. Triangulation supports agricultural spread of the Transeurasian languages. Nature. 2021;599:616–21.
- Zou Y, Tan J, Zhou J, Huang Z, Yu X, Han K, et al. Ancient genomes from the Yellow River Bend reveal long-distance population interactions between the Central Plains, Steppe, and southern China. Cell Rep. 2025;44:116034.
- McColl H, Racimo F, Vinner L, Demeter F, Gakuhari T, Moreno-Mayar JV, et al. The prehistoric peopling of Southeast Asia. Science. 2018;361:88–92.
- Allentoft ME, Sikora M, Sjogren KG, Rasmussen S, Rasmussen M, Stenderup J, et al. Population genomics of bronze age Eurasia. Nature. 2015;522:167–72.
- Liu Y, Miao B, Li W, Hu X, Bai F, Abuduresule Y, et al. Bronze Age cheese reveals human-Lactobacillus interactions over evolutionary history. Cell. 2024;187(5891–5900):e5898.
- Cai DW, Zheng Y, Bao QC, Hu XN, Chen WH, Zhang F, Cao JE, Ning C: Ancient DNA sheds light on the origin and migration patterns of the Xianbei confederation. Archaeological and Anthropological Sciences. 2023;15.
- Kumar V, Wang W, Zhang J, Wang Y, Ruan Q, Yu J, et al. Bronze and iron age population movements underlie Xinjiang population history. Science. 2022;376:62–9.
- Damgaard PB, Marchi N, Rasmussen S, Peyrot M, Renaud G, Korneliussen T, et al. 137 ancient human genomes from across the Eurasian steppes. Nature. 2018;557:369–74.
- Betts A, Jia P, Abuduresule I. A new hypothesis for early Bronze Age cultural diversity in Xinjiang, China. Archaeol Res Asia. 2018;17:204–13.
- Fällman F. The cultures of ancient Xinjiang, Western China: crossroads of the silk roads. Asian Ethn. 2020;22:208–11.
- Zhang F, Ning C, Scott A, Fu Q, Bjorn R, Li W, et al. The genomic origins of the Bronze Age Tarim Basin mummies. Nature. 2021;599:256–61.
- Hemphill BE, Mallory JP. Horse-mounted invaders from the Russo-Kazakh steppe or agricultural colonists from western Central Asia? A craniometric investigation of the Bronze Age settlement of Xinjiang. Am J Phys Anthropol. 2004;124:199–222.
- Wang W, Ding M, Gardner JD, Wang Y, Miao B, Guo W, Wu X, Ruan Q, Yu J, Hu X, et al: Ancient Xinjiang mitogenomes reveal intense admixture with high genetic diversity. Sci Adv. 2021;7.
- Zhang F, Gao S, Zhao X, Wu Y, Zhang J, Li J, et al. Bronze and Iron Age genomes reveal the integration of diverse ancestries in the Tarim Basin. Curr Biol. 2025;35(3759–3766):e3754.
- Ning C, Wang CC, Gao S, Yang Y, Zhang X, Wu X, et al. Ancient Genomes Reveal Yamnaya-Related Ancestry and a Potential Source of Indo-European Speakers in Iron Age Tianshan. Curr Biol. 2019;29(2526–2532):e2524.
- Jeong C, Wang K, Wilkin S, Taylor WTT, Miller BK, Bemmann JH, et al. A Dynamic 6,000-Year Genetic History of Eurasia’s Eastern Steppe. Cell. 2020;183(890–904):e829.
- Jeong C, Wilkin S, Amgalantugs T, Bouwman AS, Taylor WTT, Hagan RW, et al. Bronze age population dynamics and the rise of dairy pastoralism on the eastern Eurasian steppe. Proc Natl Acad Sci USA. 2018;115:E11248-55.
- Cai D, Zheng Y, Bao Q, Hu X, Chen W, Zhang F, et al. Ancient DNA sheds light on the origin and migration patterns of the Xianbei confederation. Archaeol Anthropol Sci. 2023;15:194.
- Yang XM, Meng HL, Zhang JL, Yu Y, Allen E, Xia ZY, et al. Ancient genome of Empress Ashina reveals the Northeast Asian origin of Gokturk Khanate. J Syst Evol. 2023;61:1056–64.
- Du P, Zhu K, Qiao H, Zhang J, Meng H, Huang Z, et al. Ancient genome of the Chinese Emperor Wu of Northern Zhou. Curr Biol. 2024;34(1587–1595):e1585.
- Li X, Wang M, Su H, Duan S, Sun Y, Chen H, et al. Evolutionary history and biological adaptation of Han Chinese people on the Mongolian Plateau. hLife. 2024;2(6):296–313.
- Wang M, Huang Y, Liu K, Wang Z, Zhang M, Yuan H, Duan S, Wei L, Yao H, Sun Q, et al: Multiple Human Population Movements and Cultural Dispersal Events Shaped the Landscape of Chinese Paternal Heritage. Mol Biol Evol. 2024;41.
- Wang Z, Liu K, Yuan H, Duan S, Liu Y, Luo L, Jiang X, Chen S, Wei L, Tang R, et al: YanHuang Paternal Genomic Resource Suggested A Weakly-Differentiated Multi-Source Admixture Model for the Formation of Han’s Founding Ancestral Lineages. Genomics Proteomics Bioinformatics. 2025.
- He G, Chen J, Duan S, Yang Q, Li B, Luo L, et al. Largest-scale genomic resource reconstructing the genetic origin, population structure, and biological adaptations of the Hui people. Mol Biol Evol. 2025. https://doi.org/10.1093/molbev/msaf225.
- Ning C, Fernandes D, Changmai P, Flegontova O, Yüncü E, Maier R, Altınışık NE, Kassian AS, Krause J, Lalueza-Fox C, et al: The genomic formation of First American ancestors in East and Northeast Asia. bioRxiv 2020:2020.2010.2012.336628.
- Wang R, Zhu L, Ma H, Song M, Ma G, Wang B, et al. Genetic formation of Neolithic Hongshan people and demic expansion of Hongshan culture inferred from ancient human genomes. Mol Biol Evol. 2025. https://doi.org/10.1093/molbev/msaf139.
- Zhu KY, Zhang ZP, Tao L, Jiang RQ, Huang WB, Sun YG, et al. The genetic diversity in the ancient human population of Upper Xiajiadian culture. J Syst Evol. 2024;62:785–93.
- Gelabert P, Blazyte A, Chang Y, Fernandes DM, Jeon S, Hong JG, et al. Northeastern Asian and Jomon-related genetic structure in the Three Kingdoms period of Gimhae, Korea. Curr Biol. 2022;32(3232–3244):e3236.
- Cooke NP, Mattiangeli V, Cassidy LM, Okazaki K, Stokes CA, Onbe S, et al. Ancient genomics reveals tripartite origins of Japanese populations. Sci Adv. 2021;7:eabh2419.
- Liu J, Liu Y, Zhao Y, Zhu C, Wang T, Zeng W, et al. East Asian gene flow bridged by northern coastal populations over past 6000 years. Nat Commun. 2025;16:1322.
- Cooke NP, Murray M, Cassidy LM, Mattiangeli V, Okazaki K, Kasai K, et al. Genomic imputation of ancient Asian populations contrasts local adaptation in pre- and post-agricultural Japan. iScience. 2024;27:110050.
- Aldenderfer M. Peopling the Tibetan plateau: insights from archaeology. High Alt Med Biol. 2011;12:141–7.
- d’Alpoim Guedes J, Aldenderfer M. The archaeology of the early Tibetan Plateau: new research on the initial peopling through the early Bronze Age. J Archaeol Res. 2019;28:339–92.
- Zhang XL, Ha BB, Wang SJ, Chen ZJ, Ge JY, Long H, et al. The earliest human occupation of the high-altitude Tibetan Plateau 40 thousand to 30 thousand years ago. Science. 2018;362:1049–51.
- Chen FH, Dong GH, Zhang DJ, Liu XY, Jia X, An CB, et al. Agriculture facilitated permanent human occupation of the Tibetan Plateau after 3600 B.P. Science. 2015;347:248–50.
- Meyer MC, Aldenderfer MS, Wang Z, Hoffmann DL, Dahl JA, Degering D, et al. Permanent human occupation of the central Tibetan Plateau in the early Holocene. Science. 2017;355:64–7.
- Lu D, Lou H, Yuan K, Wang X, Wang Y, Zhang C, et al. Ancestral origins and genetic history of Tibetan highlanders. Am J Hum Genet. 2016;99:580–94.
- Qi X, Cui C, Peng Y, Zhang X, Yang Z, Zhong H, et al. Genetic evidence of paleolithic colonization and neolithic expansion of modern humans on the tibetan plateau. Mol Biol Evol. 2013;30:1761–78.
- Bai F, Liu Y, Wangdue S, Wang T, He W, Xi L, et al. Ancient genomes revealed the complex human interactions of the ancient western Tibetans. Curr Biol. 2024;34(2594–2605):e2597.
- Yang X, Gao Y, Wangdue S, Ran J, Wang Q, Chen S, et al. Lake-centred sedentary lifestyle of early Tibetan Plateau Indigenous populations at high elevation 4,400 years ago. Nat Ecol Evol. 2024;8:2297–308.
- Wang H, Yang MA, Wangdue S, Lu H, Chen H, Li L, et al. Human genetic history on the Tibetan Plateau in the past 5100 years. Sci Adv. 2023;9:eadd5582.
- Liu CC, Witonsky D, Gosling A, Lee JH, Ringbauer H, Hagan R, et al. Ancient genomes from the Himalayas illuminate the genetic history of Tibetans and their Tibeto-Burman speaking neighbors. Nat Commun. 2022;13:1203.
- Jeong C, Ozga AT, Witonsky DB, Malmstrom H, Edlund H, Hofman CA, et al. Long-term genetic stability and a high-altitude East Asian origin for the peoples of the high valleys of the Himalayan arc. Proc Natl Acad Sci U S A. 2016;113:7485–90.
- Zhu K, Du P, Li J, Zhang J, Hu X, Meng H, et al. Cultural and demic co-diffusion of Tubo Empire on Tibetan Plateau. iScience. 2022;25:105636.
- Lu H, Zhang J, Liu KB, Wu N, Li Y, Zhou K, et al. Earliest domestication of common millet (Panicum miliaceum) in East Asia extended to 10,000 years ago. Proc Natl Acad Sci U S A. 2009;106:7367–72.
- Tao L, Yuan H, Zhu K, Liu X, Guo J, Min R, et al. Ancient genomes reveal millet farming-related demic diffusion from the Yellow River into southwest China. Curr Biol. 2023;33(4995–5002):e4997.
- Zhang F, Zheng L, Lv H, Duan C, Ma P, Liu Z, et al. Ancient genome analyses shed light on the origin and kinship among humans of a cliff tomb from southwestern China. J Archaeol Sci Rep. 2024;53:104333.
- Fan S, Hansen ME, Lo Y, Tishkoff SA. Going global by adapting local: a review of recent human adaptation. Science. 2016;354:54–9.
- Barrie W, Yang Y, Irving-Pease EK, Attfield KE, Scorrano G, Jensen LT, et al. Elevated genetic risk for multiple sclerosis emerged in steppe pastoralist populations. Nature. 2024;625:321–8.
- Akbari A, Barton AR, Gazal S, Li Z, Kariminejad M, Perry A, Zeng Y, Mittnik A, Patterson N, Mah M, et al: Pervasive findings of directional selection realize the promise of ancient DNA to elucidate human adaptation. bioRxiv 2024.
- Kerner G, Neehus AL, Philippot Q, Bohlen J, Rinchai D, Kerrouche N, et al. Genetic adaptation to pathogens and increased risk of inflammatory disorders in post-Neolithic Europe. Cell Genom. 2023;3:100248.
- Mathieson I, Lazaridis I, Rohland N, Mallick S, Patterson N, Roodenberg SA, et al. Genome-wide patterns of selection in 230 ancient Eurasians. Nature. 2015;528:499–503.
- Quintana-Murci L. Human immunology through the lens of evolutionary genetics. Cell. 2019;177:184–99.
- Marnetto D, Pankratov V, Mondal M, Montinaro F, Parna K, Vallini L, et al. Ancestral genomic contributions to complex traits in contemporary Europeans. Curr Biol. 2022;32(1412–1419):e1413.
- Racimo F, Marnetto D, Huerta-Sanchez E. Signatures of archaic adaptive introgression in present-day human populations. Mol Biol Evol. 2017;34:296–317.
- Gao Y, Yang X, Chen H, Tan X, Yang Z, Deng L, et al. A pangenome reference of 36 Chinese populations. Nature. 2023;619:112–21.
- Kerner G, Choin J, Quintana-Murci L. Ancient DNA as a tool for medical research. Nat Med. 2023;29:1048–51.
- Zeberg H, Paabo S. The major genetic risk factor for severe COVID-19 is inherited from Neanderthals. Nature. 2020;587:610–2.
- Orlando L, Allaby R, Skoglund P, Sarkissian CD, Stockhammer PW, Avila-Arcos MC, Fu QM, Krause J, Willerslev E, Stone AC, Warinner C: Ancient DNA analysis. Nature Reviews Methods Primers. 2021;1.
- Giguet-Covex C, Pansu J, Arnaud F, Rey PJ, Griggo C, Gielly L, et al. Long livestock farming history and human landscape shaping revealed by lake sediment DNA. Nat Commun. 2014;5:3211.
- Peters C, Richter KK, Svenning JC, Boivin N. Leveraging palaeoproteomics to address conservation and restoration agendas. iScience. 2022;25:104195.
- Yang Q, Sun Y, Duan S, Nie S, Liu C, Deng H, Wang M, He G: High-quality Population-specific Haplotype-resolved Reference Panel in the Genomic and Pangenomic Eras. Genomics Proteomics Bioinformatics. 2025.
- Sousa da Mota B, Rubinacci S, Cruz Davalos DI, CE GA, Sikora M, Johannsen NN, Szmyt MH, Wlodarczak P, Szczepanek A, Przybyla MM, et al: Imputation of ancient human genomes. Nat Commun. 2023;14:3660.
- Hui R, D’Atanasio E, Cassidy LM, Scheib CL, Kivisild T. Evaluating genotype imputation pipeline for ultra-low coverage ancient genomes. Sci Rep. 2020;10:18542.
- Tretmanis JM, Jay F, Avila-Arcos MC, Huerta-Sanchez E. Simulation-based benchmarking of ancient haplotype inference for detecting population structure. bioRxiv. 2023.
- Wang K, Tobias B, Pany-Kucera D, Berner M, Eggers S, Gnecchi-Ruscone GA, et al. Ancient DNA reveals reproductive barrier despite shared Avar-period culture. Nature. 2025;638:1007–14.
- Li YC, Tian JY, Liu FW, Yang BY, Gu KS, Rahman ZU, et al. Neolithic millet farmers contributed to the permanent settlement of the Tibetan Plateau by adopting barley agriculture. Natl Sci Rev. 2019;6:1005–13.
- He G, Liu C, Wang M. Perspectives and opportunities in forensic human, animal, and plant integrative genomics in the pangenome era. Forensic Sci Int. 2025;367:112370.
- Childebayeva A, Zavala EI. Review: computational analysis of human skeletal remains in ancient DNA and forensic genetics. iScience. 2023;26:108066.
- Blocher J, Brami M, Feinauer IS, Stolarczyk E, Diekmann Y, Vetterdietz L, et al. Descent, marriage, and residence practices of a 3,800-year-old pastoral community in Central Eurasia. Proc Natl Acad Sci U S A. 2023;120:e2303574120.
- Sikora M, Seguin-Orlando A, Sousa VC, Albrechtsen A, Korneliussen T, Ko A, et al. Ancient genomes show social and reproductive behavior of early Upper Paleolithic foragers. Science. 2017;358:659–62.
- Yaka R, Mapelli I, Kaptan D, Dogu A, Chylenski M, Erdal OD, et al. Variable kinship patterns in Neolithic Anatolia revealed by ancient genomes. Curr Biol. 2021;31(2455–2468):e2418.
- Wang J, Yan S, Li Z, Zan J, Zhao Y, Zhao J, et al. Ancient DNA reveals a two-clanned matrilineal community in Neolithic China. Nature. 2025. https://doi.org/10.1038/s41586-025-09103-x.
- Byrska-Bishop M, Evani US, Zhao X, Basile AO, Abel HJ, Regier AA, et al. High-coverage whole-genome sequencing of the expanded 1000 Genomes Project cohort including 602 trios. Cell. 2022;185(3426–3440):e3419.
- Almarri MA, Bergstrom A, Prado-Martinez J, Yang F, Fu B, Dunham AS, et al. Population Structure, Stratification, and Introgression of Human Structural Variation. Cell. 2020;182(189–199):e115.
- Wang W, Ding M, Gardner JD, Wang Y, Miao B, Guo W, et al. Ancient Xinjiang mitogenomes reveal intense admixture with high genetic diversity. Sci Adv. 2021;7:eabd6690.
- Alexander DH, Novembre J, Lange K. Fast model-based estimation of ancestry in unrelated individuals. Genome Res. 2009;19:1655–64.
- Chang CC, Chow CC, Tellier LC, Vattikuti S, Purcell SM, Lee JJ. Second-generation PLINK: rising to the challenge of larger and richer datasets. Gigascience. 2015;4:7.
- Patterson N, Moorjani P, Luo Y, Mallick S, Rohland N, Zhan Y, et al. Ancient admixture in human history. Genetics. 2012;192:1065–93.
- Zhao D, Chen Y, Xie G, Ma P, Wen Y, Zhang F, et al. A multidisciplinary study on the social customs of the Tang Empire in the Medieval Ages. PLoS One. 2023;18:e0288128.
- Shen Q, Wu Z, Zan J, Yang X, Guo J, Ji Z, et al. Ancient genomes illuminate the demographic history of Shandong over the past two millennia. J Genet Genomics. 2025;52:494–501.
- Maa H, Zhoub Y, Wanga R, Yanc F, Chena H, Qiua L, et al. Ancient genomes shed light on the long-term genetic stability in the central plain of China. Sci Bull. 2024;7:e24.
- Jonsson H, Ginolhac A, Schubert M, Johnson PL, Orlando L. MapDamage2.0: fast approximate Bayesian estimates of ancient DNA damage parameters. Bioinformatics. 2013;29:1682–4.
- He G, Sun Y, Duan S, Luo L, Sun Q, Li B, Yun L, Liu C, Wang M: Data for research article “Ancient genomes give insight into 160,000 years of East Asian population dynamics and biological adaptation”. Zenodo 2025. https://zenodo.org/records/17270846.
- He G, Sun Y, Duan S, Luo L, Sun Q, Li B, Yun L, Liu C, Wang M: Code for research article “Ancient genomes give insight into 160,000 years of East Asian population dynamics and biological adaptation”. Zenodo 2025. https://zenodo.org/records/17270850.
- He G, Sun Y, Duan S, Luo L, Sun Q, Li B, Yun L, Liu C, Wang M: Code for review “Ancient genomes give insight into 160,000 years of East Asian population dynamics and biological adaptation”. Zenodo 2025. https://doi.org/10.5281/zenodo.17271668.